动脉粥样硬化(AS)是一种常见的血管性疾病,发病率和死亡率都较高,其发病机制相当复杂,目前尚无有效的治疗策略。而冠状动脉内的血管平滑肌细胞(VSMCs)的表型转化、增殖、衰老和凋亡影响AS的发生。另外,环状RNA通过调节内皮细胞(ECs)、VSMCs和巨噬细胞的功能,与AS的病理生理过程有关。敲除circUSP9X可促进细胞周期和血管生成,抑制细胞凋亡、氧化应激以及ECs的炎症反应。那么circUSP9X是否能够通过调节VSMCs的功能进而影响AS病理生理过程呢?
2023年11月3日,浙江中医药大学嘉兴学院联合培养基地和嘉兴大学附属医院第一医院心血管内科钱钢主任团队在Clinical and Experimental Hypertension(IF=12.3)发表文章”CircUsp9x/miR-599/STIM1 axis regulates proliferation and migration in vascular smooth muscle cells induced by oxidized-low density lipoprotein”。本研究表明在AS和ox-LDL诱导的VSMCs中,circUSP9X和STIM1水平表达上调,miR-599水平表达下调。在功能上,circUSP9X通过miR-599/STIM1轴促进氧化-低密度脂蛋白(ox-LDL)诱导的VSMCs的增殖和迁移。研究结果提示,circUSP9X/miR-599/STIM1轴具有AS治疗的潜力。

CircUSP9X在AS和ox-LDL治疗的VSMCs患者中表达上调
首先,作者检测了AS患者和健康个体的血清样本中circUSP9X的水平,发现AS患者血清中circUSP9X的表达明显升高(图1a)。另外,分别用0、25、50、75和100 μg/mL的ox-LDL处理VSMCs 24h并进行细胞活力评估。结果显示,细胞活力以剂量依赖性的方式得到促进(图1b)。接着选择最显著剂量的ox-LDL(75 μg/ml)治疗VSMCs 0、12、24和48 h,发现ox-LDL时间依赖性的方式促进细胞活力(图1c)。此外,在ox-LDL诱导的VSMCs中检测到circUSP9X的表达。且ox-LDL以剂量依赖性和时间依赖性的方式增加了circUSP9X的水平(图1d,e)。
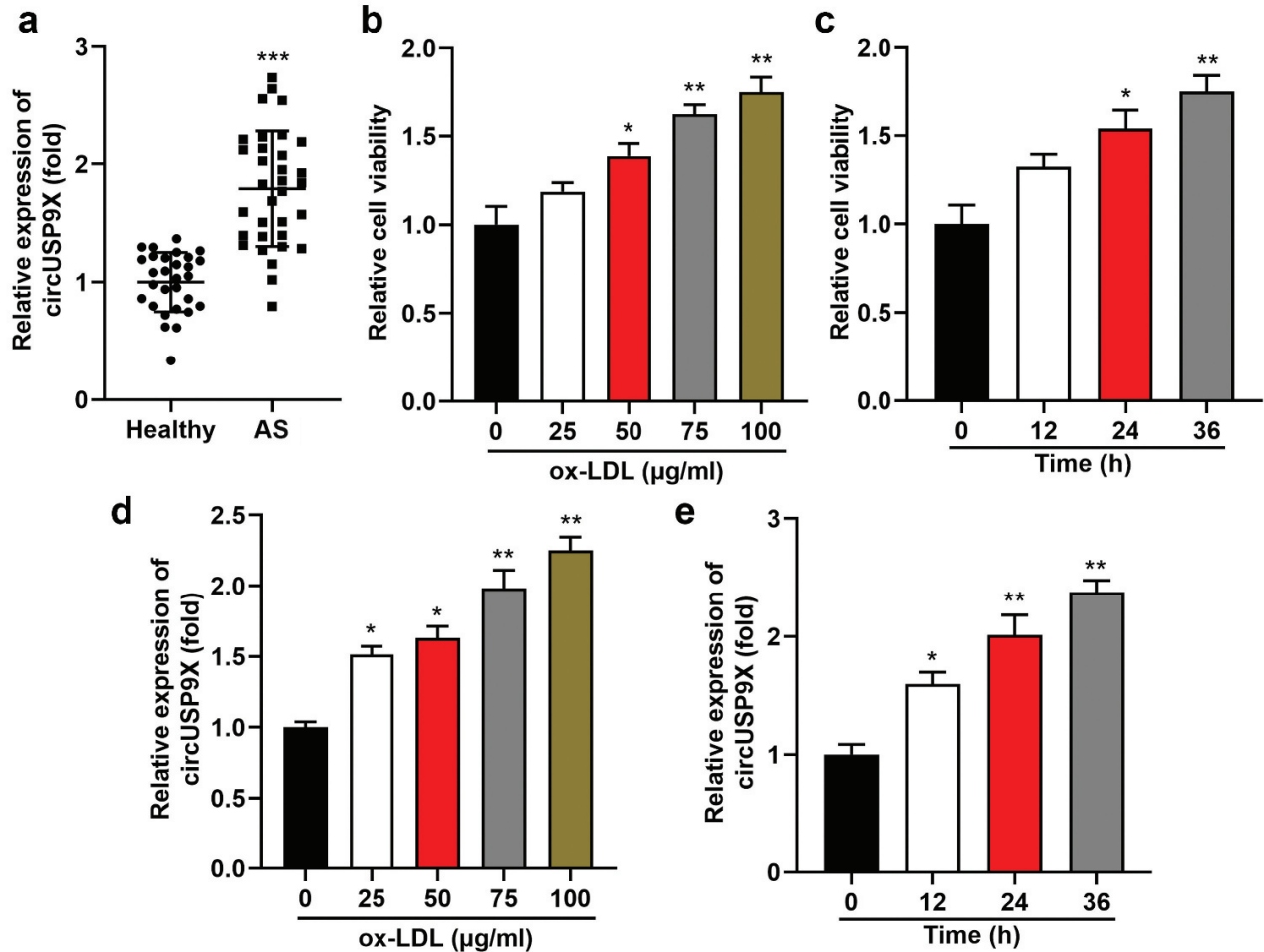
图1 CircUSP9X在AS和ox-LDL诱导的VSMCs中表达上调
CircUSP9X促进ox-LDL诱导的VSMCs的增殖和迁移
为了探讨circUSP9X的作用,作者将circUSP9X过表达载体和si-circUSP9X转染到VSMCs中。结果表明过表达circUSP9X显著促进了细胞增殖,而敲除circUSP9X则显著抑制了ox-LDL诱导的细胞增殖(图2b-d)。同时,circUSP9X显著促进了细胞迁移,而抑制circUSP9X显著阻碍了ox-LDL诱导的细胞的迁移(图2e-h)。接着作者检测了AS中VSMCs增殖标志物(CDK2、cyclineE1)和迁移标志物(MMP2、MMP9)的蛋白水平。结果显示,过表达circUSP9X上调了ox-LDL诱导的CDK2、cyclinE1、MMP2和MMP9的水平,而干扰circUSP9X则下调了它们的水平(图2i-m)。综上所述,CircUSP9X促进ox-LDL诱导的VSMCs的增殖和迁移。
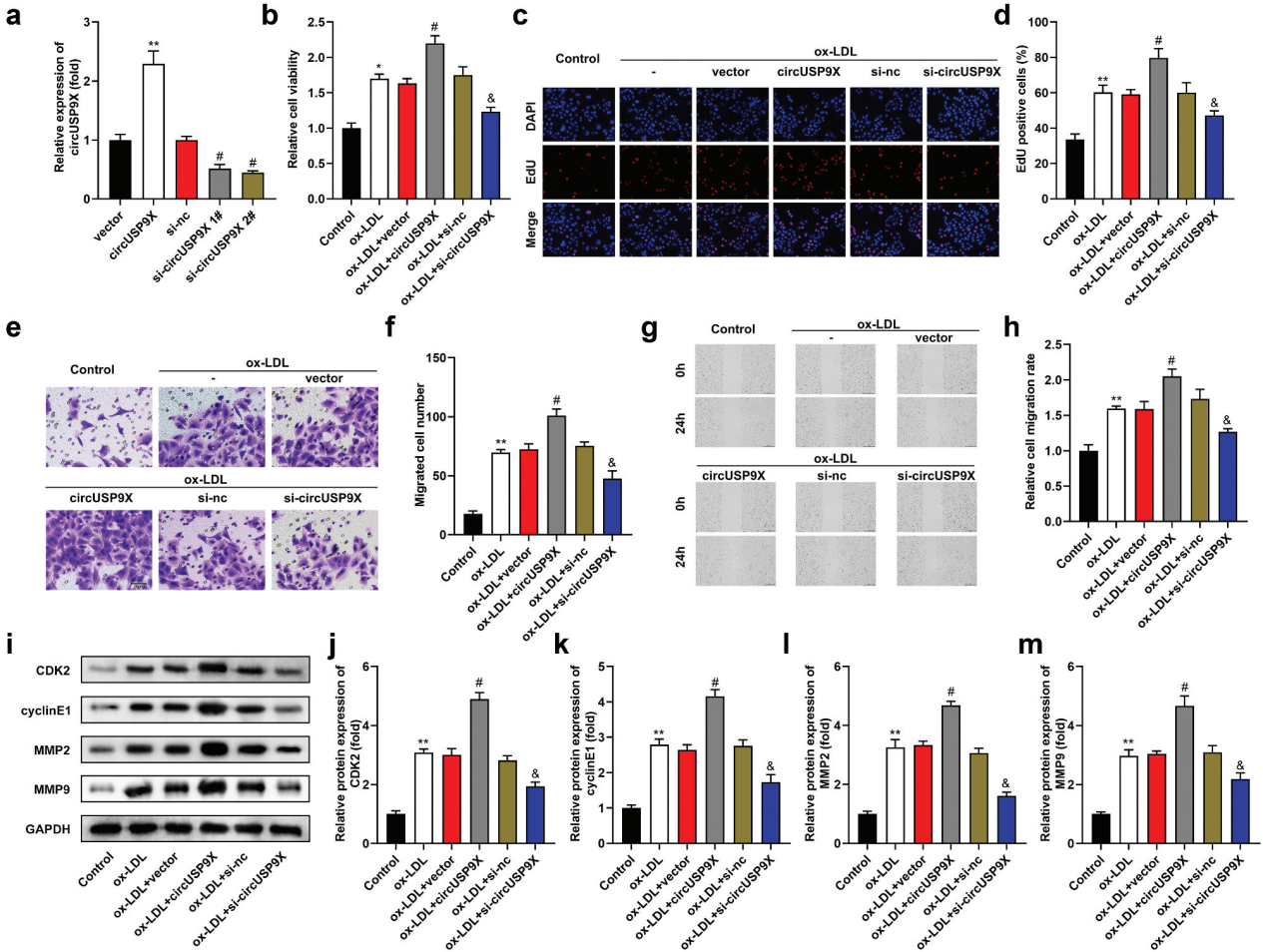
图2 CircUSP9X促进ox-LDL诱导的VSMCs的增殖和迁移
CircUSP9X海绵吸附miR-599
作者利用生物信息学方法检索了 circUSP9X 和 miR-599 之间的直接互补区域(图3a)。miR-599是AS发展中的重要调控因子。重要的是,miR-599可调节内皮损伤并影响VSMCs的增殖和迁移。所以作者选择miR-599进行进一步研究。与模拟物NC相比,与circUSP9X-wt和模拟物共转染的VSMCs的荧光素酶活性显著降低(图3b)。RNA-pulldown实验表明,生物素标记的miR-599显著降低了circUSP9X(图3c)。circUSP9X和miR-599均主要位于细胞质中(图3d)。与对照组相比,miR-599在AS患者的血清中低表达(图3e)。在AS患者中,miR-599的表达与circUSP9X的表达呈负相关(图3f)。在VSMCs中,miR-599的表达受到circUSP9X的负调控(图3g)。
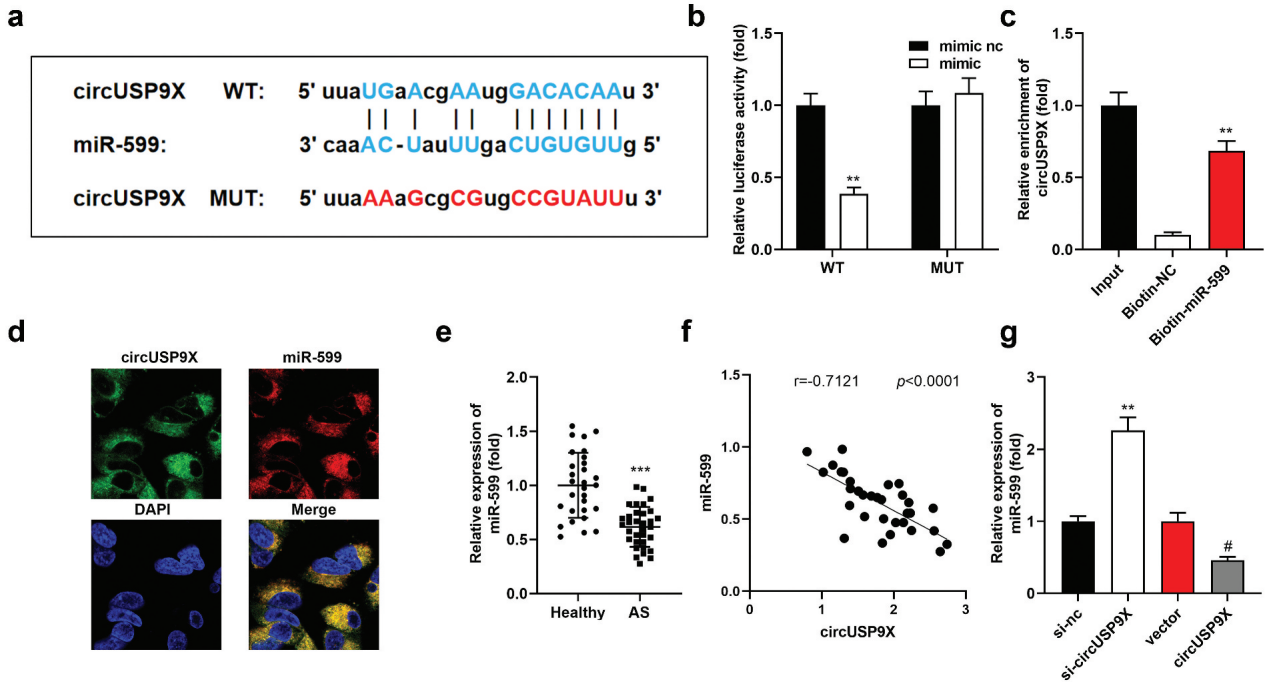
图3 CircUSP9X海绵吸附miR-599
CircUSP9X通过海绵化miR-599促进生物行为
miR-599在模拟物转染和抑制剂转染的细胞中的表达分别显著上调和降低(图4a)。circUSP9X显著促进了细胞增殖,而过表达miR-599则抑制了细胞增殖(图4b-d)。CircUSP9X显著促进了ox-LDL诱导的VSMCs迁移,而miR-599则抑制了这种促进作用(图4e-h)。此外,circUSP9X显著提高了CDK2、cyclinE1、MMP2和MMP9蛋白水平,而miR-599逆转了circUSP9X诱导的MMP9蛋白水平(图4i-m)。
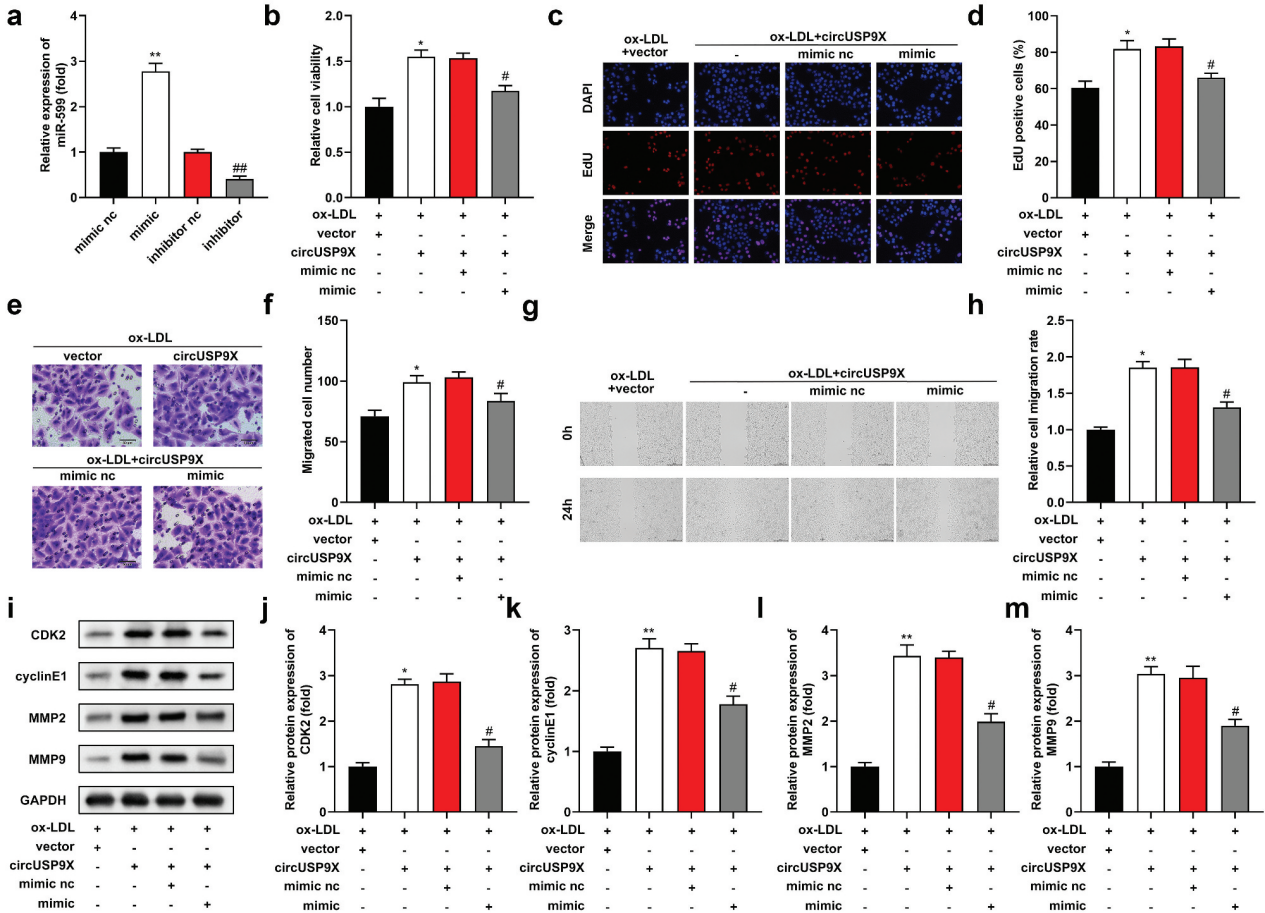
图4 CircUSP9X通过miR-599促进细胞过程
MiR-599靶向STIM1
生物信息学结果显示,miR-599与STIM1是互补的(图5a)。与模拟物NC相比,共转染STIM1-wt和mimic的VSMCs的荧光素酶活性明显降低(图5b)。生物素标记的miR-599显著拉低了STIM1(图5c)。FISH结果显示,STIM1和miR-599均位于细胞质中(图5d)。AS患者血清中STIM1的表达增加,并与miR-599呈负相关(图5e,f)。此外,STIM1的表达受到miR-599的负调控(图5g)。
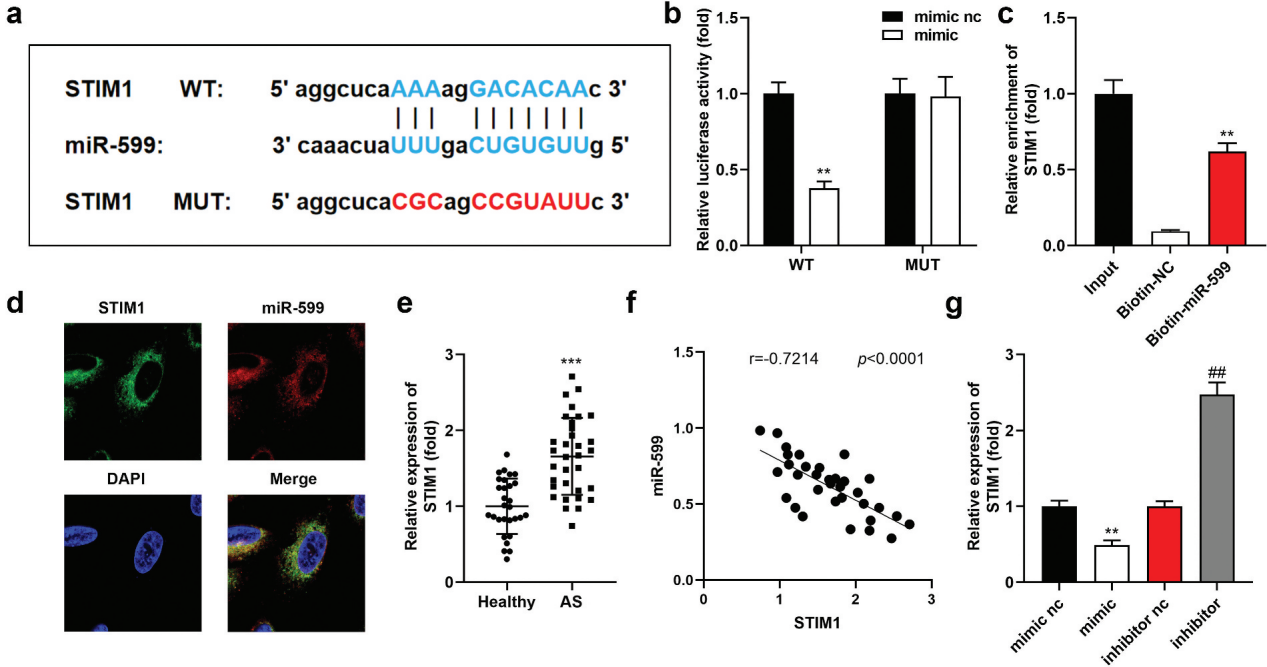
图5 MiR-599靶向STIM1
MiR-599通过靶向STIM1来抑制生物学行为
MiR-599 mimic显著抑制了细胞增殖,过表达STIM1逆转了miR-599的作用(图6b-d)。miR-599明显抑制了细胞迁移,而STIM1则减弱miR-599的抑制(图6e-h)。miR- 599显著降低了CDK2、cyclinE1、MMP2和MMP9的蛋白水平,而STIM1则消除了miR- 599的影响(图6i-m)。
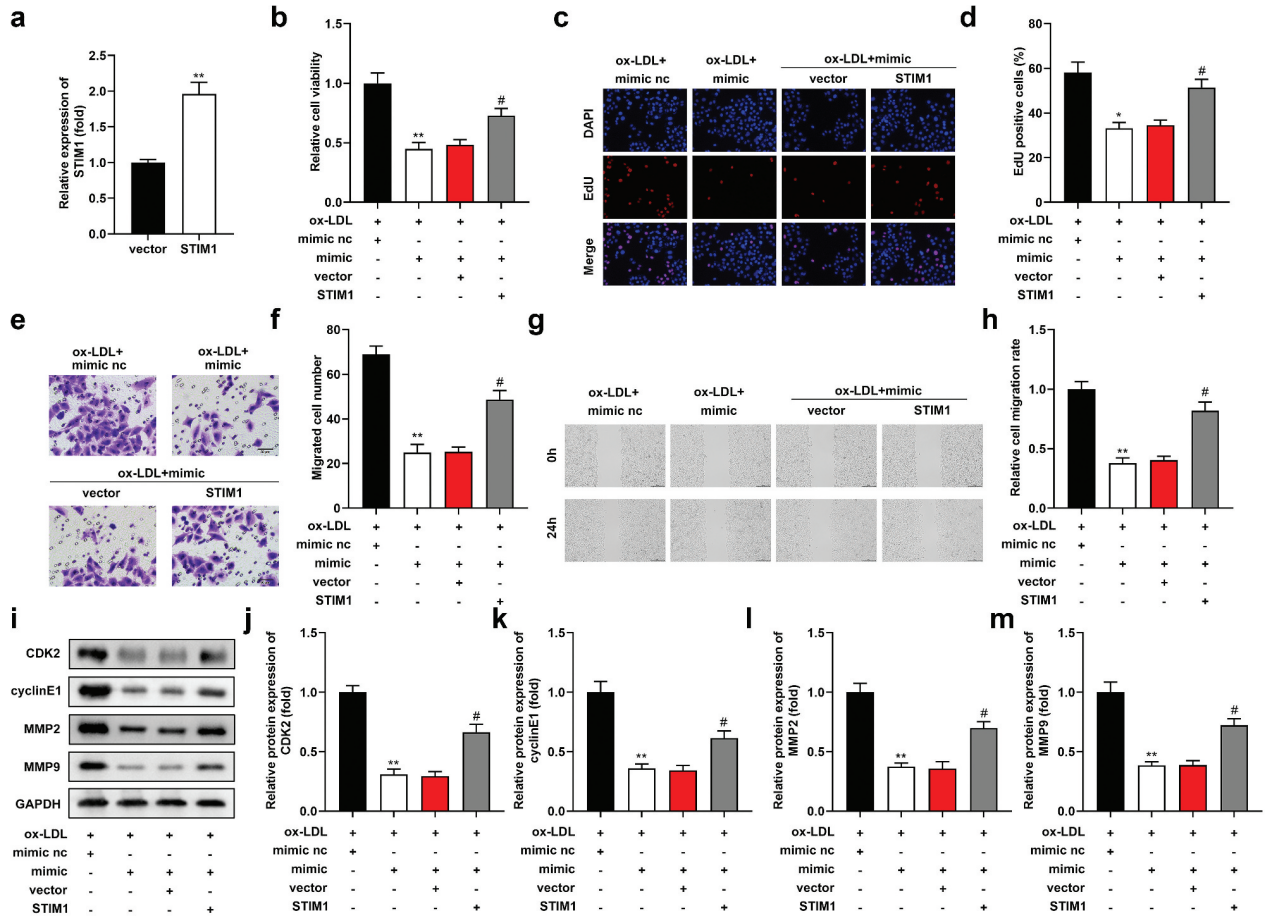
图6 MiR-599通过STIM1抑制ox-LDL诱导的生物学功能
总结
在AS和ox-LDL刺激的VSMCs患者的血清中,CircUSP9X和STIM1的表达增加,而miR-599的表达降低。过表达circUSP9X促进了ox-LDL诱导的VSMCs的增殖和迁移。CircUSP9X海绵吸附靶向STIM1的miR-599。MiR-599逆转了circUSP9X诱导的作用,而STIM1逆转了MiR-599诱导的作用。综上所述,CircUSP9X通过miR-599/STIM1轴促进ox-LDL处理的VSMCs的增殖和迁移。
文献来源
https://doi.org/10.1080/10641963.2023.2280758
.png)
