
一、PIE剪接策略合成RNase R抗性circRNA,可利用RT-PCR量化
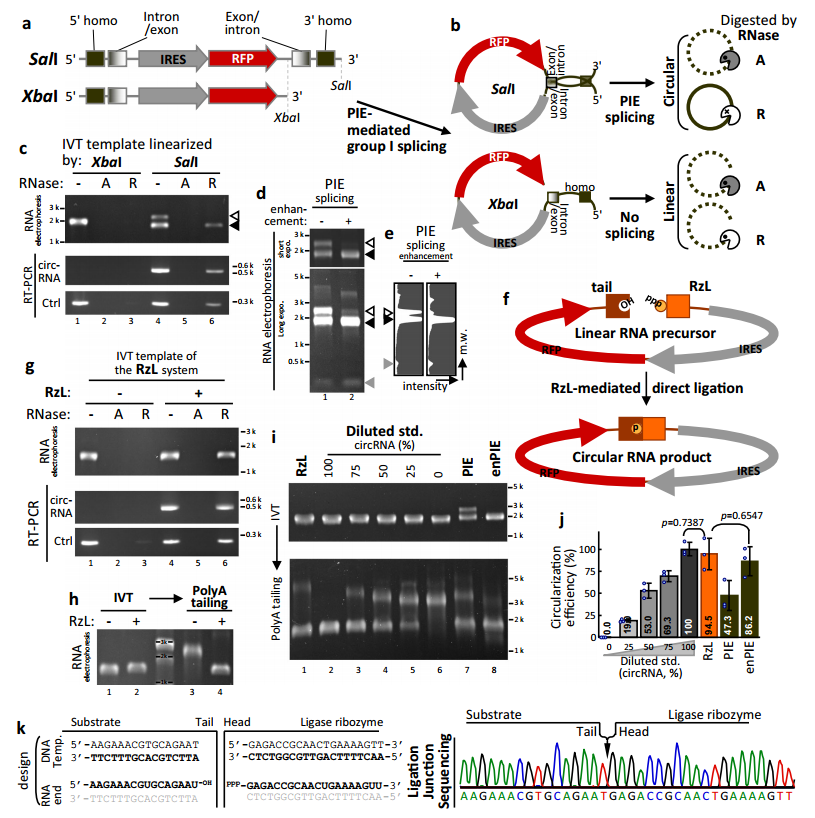
图1 传统内含子-外显子(PIE)方法以及连接酶核酶(RzL)催化circRNA生成策略的建立。
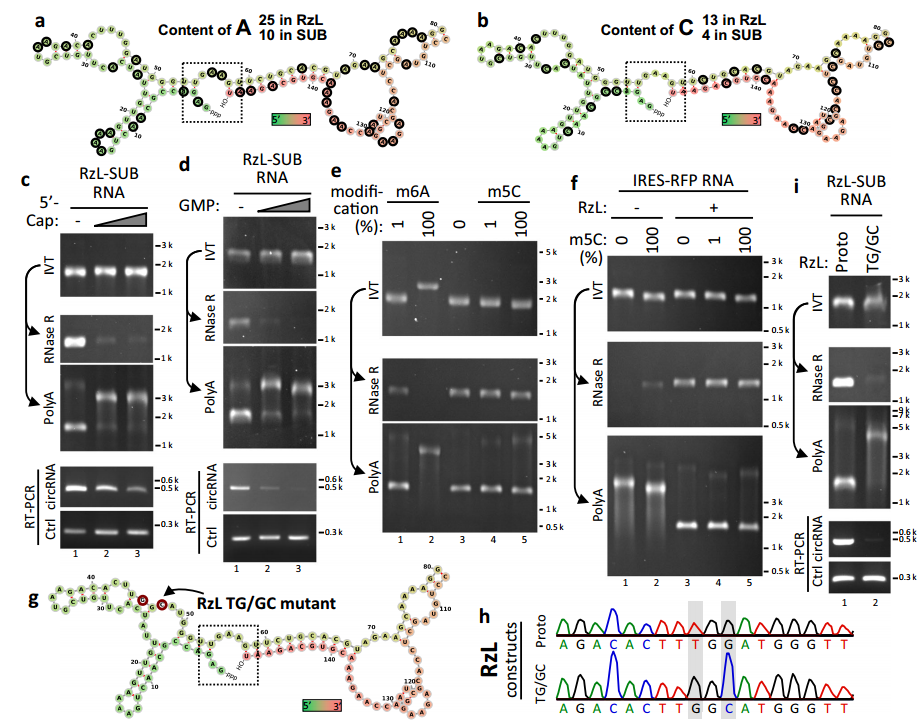
图2 RNA修饰影响RzL催化circRNA形成。
四、具有两个IRES的circRNA会阻碍彼此的蛋白表达
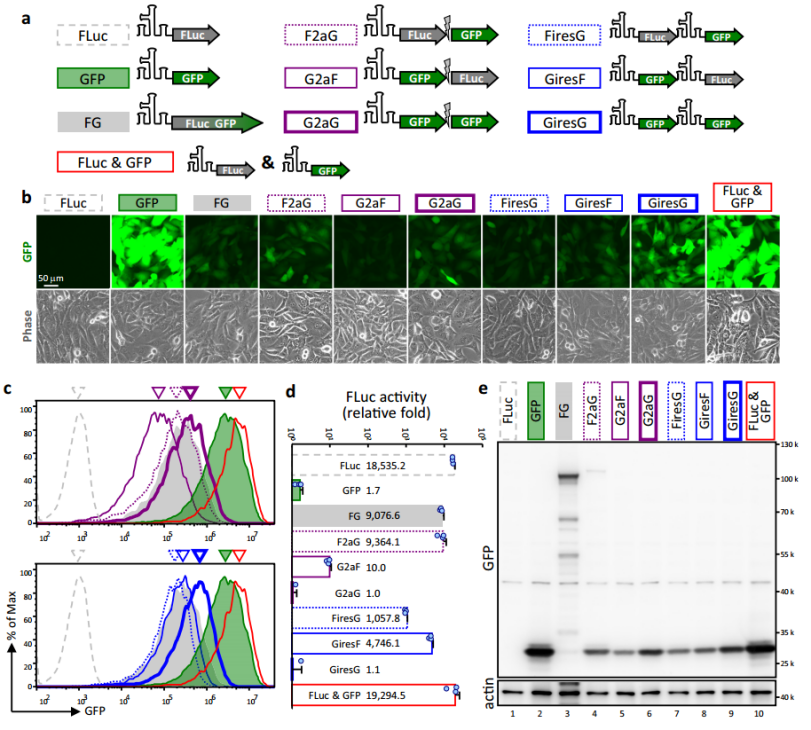
图3 外部IRES中的cis,而非trans阻碍了circRNA的翻译。
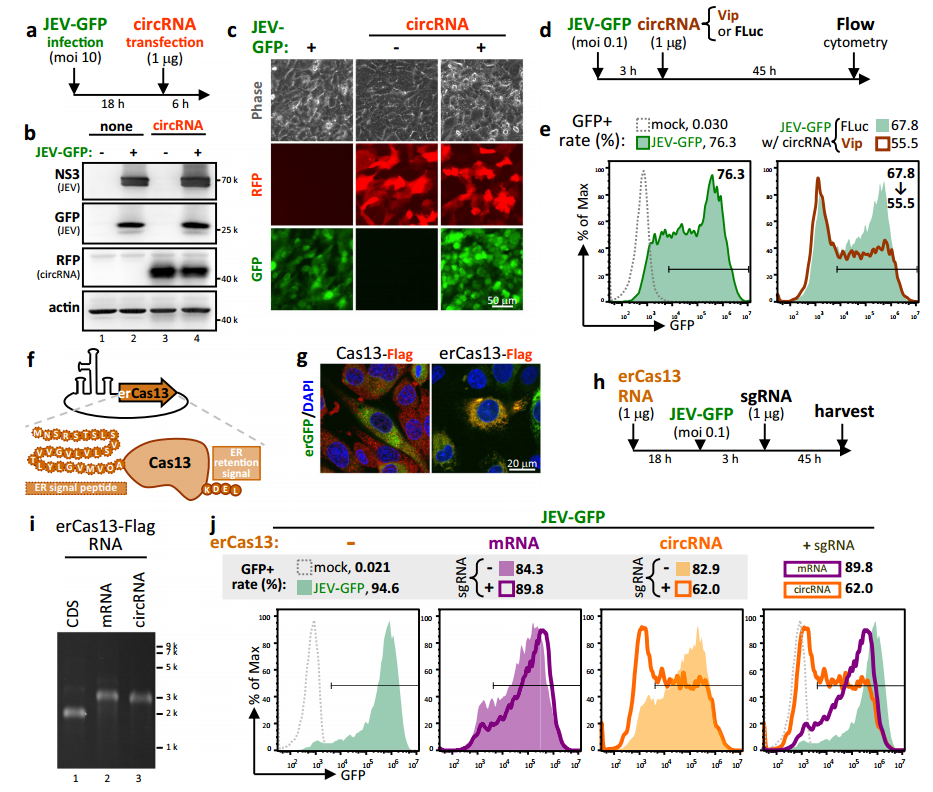
图4 IRES驱动表达erCas13的circRNA可能对重组RNA病毒JEV-GFP具有抗病毒作用。

一、PIE剪接策略合成RNase R抗性circRNA,可利用RT-PCR量化

图1 传统内含子-外显子(PIE)方法以及连接酶核酶(RzL)催化circRNA生成策略的建立。

图2 RNA修饰影响RzL催化circRNA形成。
四、具有两个IRES的circRNA会阻碍彼此的蛋白表达

图3 外部IRES中的cis,而非trans阻碍了circRNA的翻译。

图4 IRES驱动表达erCas13的circRNA可能对重组RNA病毒JEV-GFP具有抗病毒作用。