Shenjian
肿瘤微环境 (tumor microenvironment,TME) 是肿瘤细胞赖以生存和发展的复杂内部环境,TME是一个复杂的生态系统,并且在肿瘤发生的所有阶段都发挥着重要作用。TME由癌细胞,与癌症相关的成纤维细胞(CAF),内皮细胞,免疫细胞,细胞外基质(ECM),微血管和浸润的生物分子组成。其中,肿瘤微环境内的免疫细胞及其调节方式对肿瘤的发生和发展起着重要的作用,肿瘤微环境免疫特征已经被列入肿瘤十大特征之一,其一方面能够在预测患者临床预后中发挥作用;另一方面,还能预测患者临床化疗或者放疗等的临床疗效。如今,癌症免疫疗法开启了肿瘤治疗的新潮流并取得了惊人的成绩,但是,大约只有三分之一的患者受益于抗CTLA4,抗PD-1和抗PD-L1抗体在内的免疫检查点抑制剂(ICI)治疗。如何应对分子靶向药物耐药或者疗效不佳成为了广大研究者的新挑战。因此,分析肿瘤微环境中免疫细胞的种类和分布等,具有重要的临床意义。
肿瘤免疫微环境分子标记物挖掘离不开生物信息技术的迅速发展,目前,科学家已经开发了许多生物信息学工具来寻找生物标志物。比如,加权基因共表达网络分析(WGCNA)算法已被广泛用于在转录水平上寻找生物标记,可用于挖掘基因之间的相关模式,以识别癌症的相关模块和核心基因,是一种有效的工具。CIBERSORT算法通过估计RNA转录本的相对子集进行细胞类型鉴定,该工具使用解卷积算法来量化免疫细胞的细胞组成,是另一种用于分析基因表达数据的生物信息学工具。
在临床科研中,我们结合TCGA和GEO在线数据库中的肿瘤表达谱数据进行免疫浸润分析,对研究问题的解读和湿实验的指导,可起到事半功倍的作用。目前国际上也发表了不少这方面以生信分析为主湿实验为辅的研究论文。下面我们以近期在Aging (Albany NY)杂志(影响因子:5.515分)发表的一篇文章为例,给大家展示从转录组数据挖掘与肿瘤免疫微环境相关分子标记物的分析思路。

该研究的对象锁定为透明细胞肾细胞癌(ccRCC),肾细胞癌(RCC)是最常见的恶性肿瘤之一,RCC占所有肾癌的80%,而透明细胞肾细胞癌是最常见的肾细胞癌亚型。近年来,免疫检查点抑制剂已成为肾细胞癌一线治疗的标准。但是,尚无用于肾细胞癌免疫治疗的特异性分子标记。因此,探索免疫相关分子标志物是肾细胞癌研究的核心重点。RCC易于发生免疫浸润,并且肿瘤微环境的特征强烈改变了对免疫治疗的反应。CD8 + T细胞有助于肿瘤适应性免疫。在ccRCC免疫细胞中,CD8 + T细胞占最大比例。在大多数实体瘤中,高度浸润的CD8 + T细胞有利于肿瘤治疗,但RCC中CD8 + T细胞的高度浸润与不良预后有关。因此,鉴定与CD8 + T细胞浸润有关的生物标志物将有助于监测RCC免疫治疗反应和探索免疫浸润机制。
研究内容
该研究内容主要包含以下几个部分:
- GEO数据库中下载GSE73731数据,该数据集包含265 ccRCC样品的转录组表达数据;
- 挑选表达值变异系数大于0.1的4411个基因用于后续WGCNA分析;
- CIBERSORT算法评估肿瘤浸润免疫细胞(TIIC),评估每个样品的不同细胞亚型的丰度,选择每个样品中T细胞的七个亚型的分数作为WGCNA的性状数据;
- WGCNA分析构建ccRCC基因共表达网络;
- Hub枢纽模块的识别和富集分析;
- Hub基因的鉴定和验证;
- 确定免疫和临床特征;
- 鉴定预后生物标志物;
- 标记基因功能实验验证;
技术路线图:
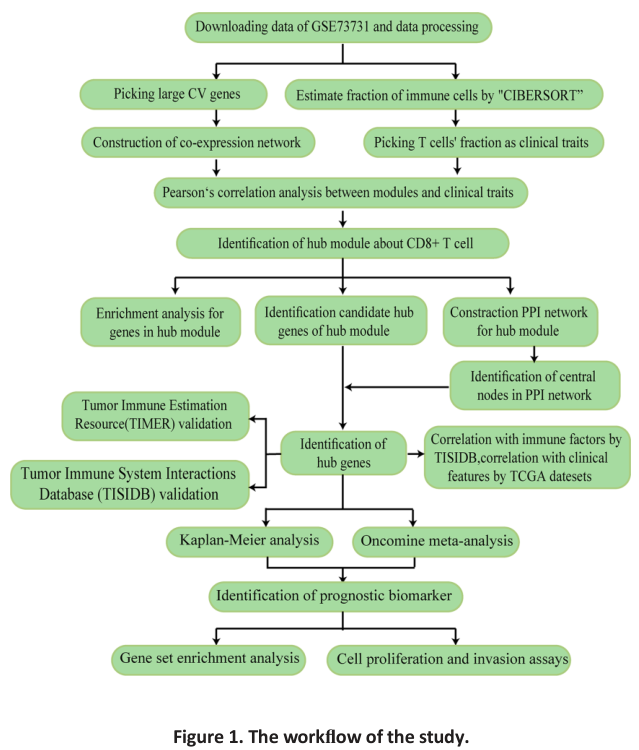
分析过程及结果展示:
1、ccRCC基因共表达网络分析
通过NCBI网站的GEO数据库(GSE73731)获取265 ccRCC样品的RNA表达数据,挑选出变异系数值大于0.1的4411个基因。CIBERSORT算法评估每个样品中不同肿瘤浸润免疫细胞(TIIC)细胞亚型的丰度,选择每个样品中T细胞的七个亚型的分数作为WGCNA的性状数据。随后,使用R包“ WGCNA”对4411个基因构建共表达网络,建立无标度网络,软阈值β= 3(R2 = 0.8723676)。使用动态混合切割构建层次聚类树。树上的每片叶子代表一个基因,具有相似表达数据的基因靠在一起,形成树的一个分支,代表一个基因模块。生成了九个模块。
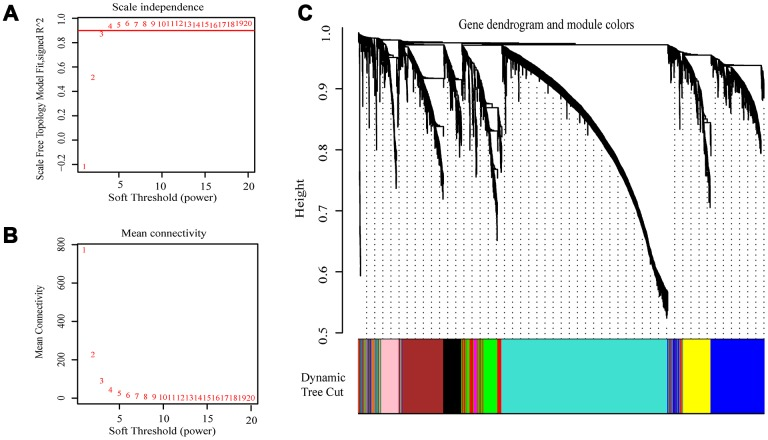
图1注:选择适当的beta值以构造层次聚类树。(A)分析1-20软阈值(β)的无标度拟合指数。(B)分析1-20软阈值功率的平均连通性。(C)基因通过层次聚类分为不同的模块,不同的颜色代表不同的模块。
2、Hub枢纽模块的识别和富集分析
WGCNA分析得到基因表达模块与肿瘤浸润免疫细胞亚型形状关联关系,在这九个模块中,绿色模块与T细胞CD8(CD8 + T细胞)(R2 = 0.5,P = 2e-18),CD4 激活记忆T细胞(R2 = 0.45,P = 1e-14),伽马δT细胞(R2 = 0.62,P = 3e-29)高度相关。黄色模块显示与CD4 激活记忆T细胞相关(R2 = 0.5,P = 4e-18)。其他模块与T细胞之间的相关性小于0.5。因此重点关注显示与CD8 + T细胞相关的绿色模块,将其识别为核心模块。接下来,使用网络工具“Matascape”分析该模块中包含的基因,进行信号通路和生物学过程富集分析。20个最显著富集的都是与免疫相关的通路,而三个最富集的是淋巴细胞激活,适应性免疫应答和细胞因子介导的信号通路。
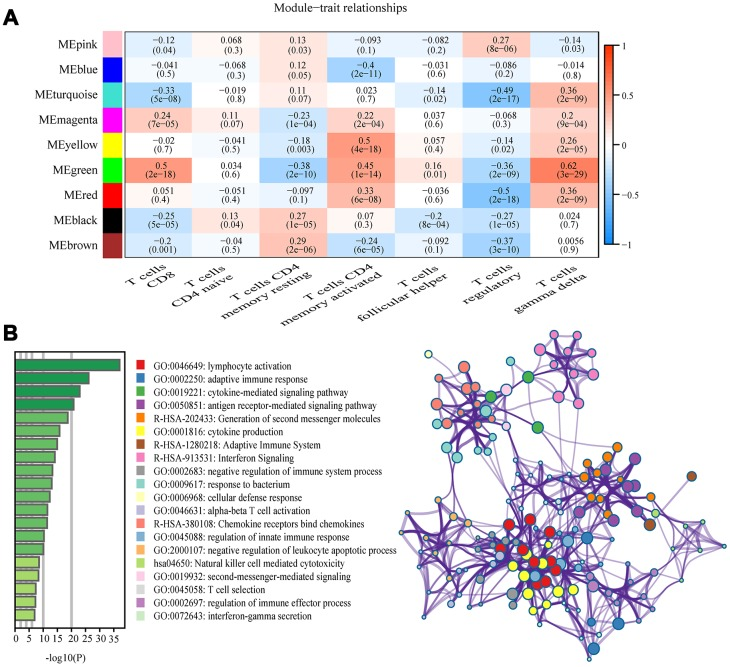
图2注:关键模块和功能说明。(A)热图显示模块特征基因与T细胞浸润的相关性。(B)基因功能富集分析,富集到的前20个GO和通路描述。右侧的网络图是将每个富集项作为一个节点,并将该节点的相似性作为边来构造的。具有相同集群ID的节点具有相同的颜色。3、Hub基因的鉴定和验证
上述选定的绿色模块包含的基因与CD8 + T细胞浸润水平高度相关的潜在关键因素。根据cut off标准(Module-Membership> 0.8,Gene-Significance> 0.5),选择了30个基因作为候选中心基因。对30个候选中心基因进行蛋白质-蛋白质相互作用(PPI)网络分析,reliability > 0.7 和connectivity > 15作为cut off,将30个基因鉴定为中心节点,使用Cytoscape可视化。在两个分析中选择了十个基因指定为中枢基因(LCK,CD2,CD3D,CD3G,IRF1,IFNG,CCR5,CD8A,CCL5和CXCL9)。为了研究这些中枢基因与CD8 + T细胞之间的关系,进一步在TIMER数据库中分析了这些基因的表达数据。结果显示10个基因的表达值与CD8 + T细胞的浸润水平呈正相关(除CXCL9外,所有其他基因的相关系数至少为0.75)。接下来,查询TISIDB数据库以获得肿瘤浸润淋巴细胞的丰度与基因表达之间的Spearman相关值。结果表明中枢基因和肿瘤浸润淋巴细胞之间呈正相关。激活的CD8 + T细胞(Act CD8)和效应记忆CD8 + T细胞(Tem CD8)的相关值最高。这些分析验证了已鉴定的hub基因与CD8 + T细胞浸润水平密切相关,并在免疫微环境中发挥重要作用。
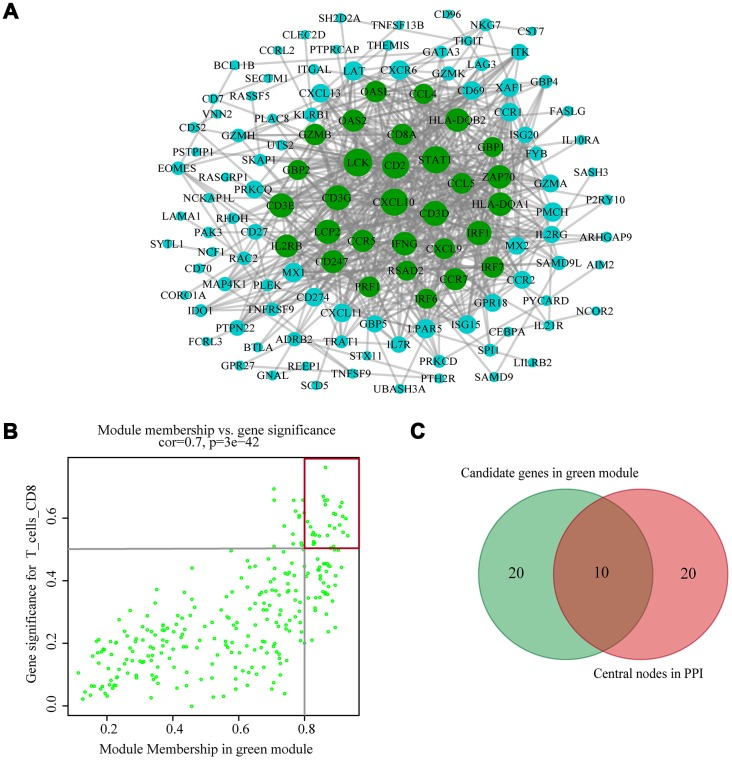
图3注:hub基因的鉴定。(A)来自绿色模块的基因的PPI网络分析。连接的节点数越多,则节点越大。绿色节点表示具有15个以上连接的中央节点。(B)绿色模块中基因的散点图。每个绿色点表示一个基因,红色框中的点表示模块reliability > 0.7 和connectivity > 15的基因。(C)基于PPI和共表达网络之间的重叠分子,选择为Hub基因。
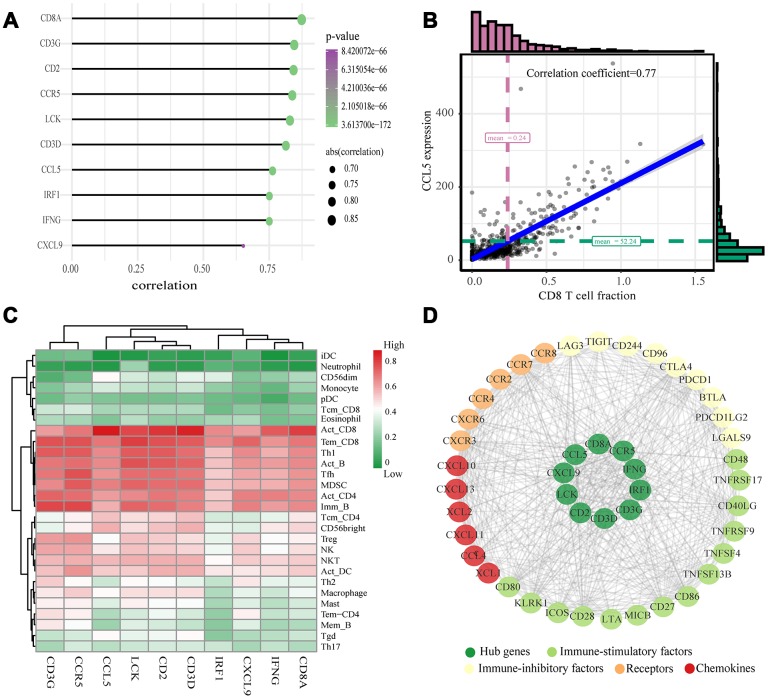
图4注:验证中枢基因和PPI图的构建。(A)10个hub基因表达与CD8 + T细胞浸润水平之间的关系;P <0.05。(B)CCL5表达和CD8 + T细胞浸润水平的散点图。(C)热图显示了十个已识别的中枢基因与TISIDB数据库中TIIC之间的相关性。红色表示相关性较高,绿色表示相关性较低。(D)ccRCC免疫微环境的蛋白质-蛋白质相互作用图。
4、确定免疫和临床相关特征
TISIDB数据库中搜索这10个中枢基因的表达与免疫因子表达的Spearman相关性,包括免疫抑制因子,免疫刺激因子,趋化因子和受体。确定了38个与免疫相关的因子,它们与10个中枢基因的平均相关性均大于0.5。利用STRING数据库探索CD8 + T细胞的浸润机制,基于10个中枢基因和38个免疫相关因子构建了一个免疫浸润相互作用网络。将结果导入Cytoscape以进行可视化。接下来,TCGA中获得了ccRCC的10个基因的表达水平。根据Wilcoxon signed-rank检验,这些基因在肿瘤组织中的表达水平高于正常组织(P <0.05)。火山图还显示,肿瘤组织中10个基因的表达显著高于正常组织中的表达。肿瘤组织中CCL5和CXCL9的倍数变化比正常组织中的水平高2.5倍以上。箱线图显示了中枢基因与病理阶段之间的关系。所有中枢基因的表达水平在病理阶段均表现出显著差异(p <0.05),并且随着阶段的增加而呈上升趋势。最后,作者研究了肿瘤级别与中枢基因之间的联系,其中LCK,CD2,CD3D,IFNG,CD8A和CCL5与不同级别肿瘤显著相关(p <0.05),级别增加对应于基因表达增加。尽管未检测到CD3G,IRF1,CCR5和CXCL9的显著差异,但随着肿瘤等级的增加,基因表达水平呈上升趋势。

图5注:TCGA的转录数据中的hub基因的差异表达。(A)LCK,蓝点代表正常组织,红点代表肿瘤组织。y轴显示基因的表达值。(B)CD2。(C)CD3D。(D)CD3G。(E)IRF1。(F)IFNG。(G)CCR5。(H)CD8A。(I)CCL5。(J)CXCL9。(K)差异表达基因的火山图。红点表示高表达基因,绿点表示低表达基因,黑圈表示hub基因。
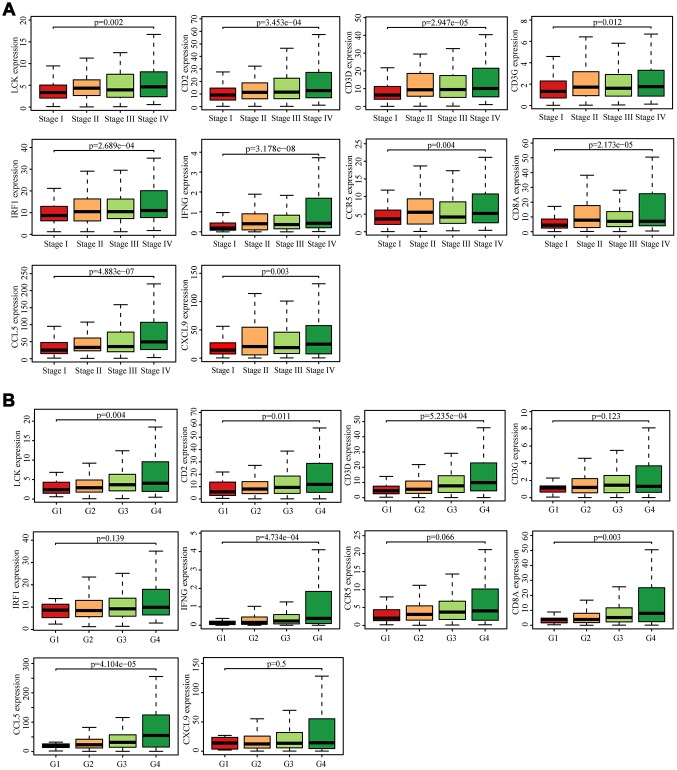
图6注:TCGA数据集中的中枢基因和临床指标分析。(A)不同病理阶段中枢基因的箱线图。(B)不同级别肿瘤的中枢基因的箱线图。
5、预后生物标志物鉴定
研究者通过Kaplan-Meier分析分析了10个中枢基因,只有CCL5和IFNG的结果具有统计学意义(p <0.05)。对于这两个基因,高表达患者的生存预后很差。为了验证肿瘤和正常组织中10个基因的差异表达,我们使用Oncomine数据库中四个数据集进行了荟萃分析,所有这些数据集均包括肿瘤组织和正常对照。这些数据集不包括IFNG的数据,因此我们获得了其他9个基因的荟萃分析结果。LCK,CD2,CD3D,CCR5,CCL5和CXCL9的中位秩值小于1000,CD3G为3007.0,IRF1为1445.0,CD8A为1577.0。结果表明这些基因在肿瘤组织中表现出明显的高表达,这与TCGA数据集分析相一致。通过Kaplan-Meier和Oncomine荟萃分析,我们选择CCL5作为进一步分析的预后生物标志物。
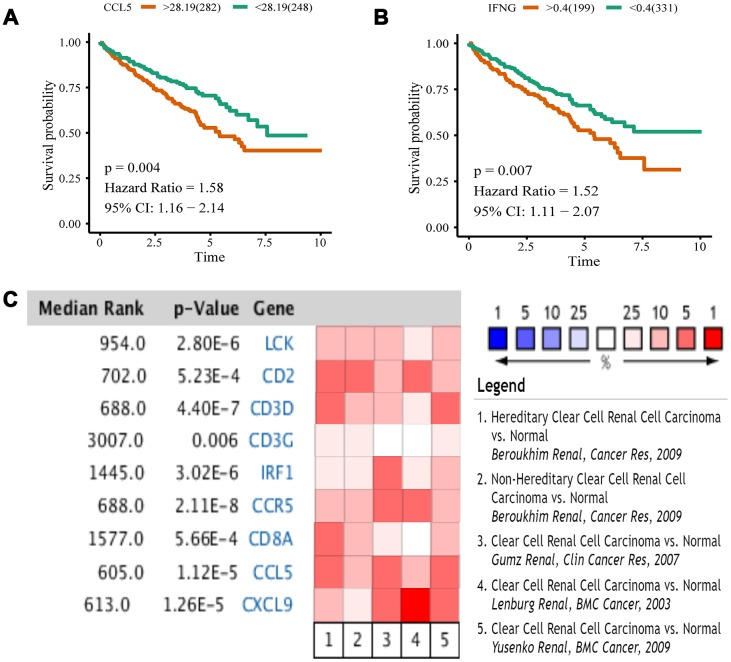
图7注:Kaplan-Meier生存分析和Oncomine meta分析。(A)CCL5的整体生存分析。(B)IFNG的整体生存分析。(C)来自Oncomine数据集的基因表达的meta分析。彩色方块代表五个数据集中基因的中位数(相对于正常组织)。红色表示高表达,蓝色表示低表达。
6、CCL5基因集富集分析
根据CCL5表达中值,将TCGA的ccRCC样品分为高表达组和低表达组,然后对基因集进行通路富集分析。富集结果表明,高表达组中免疫相关的途径被富集,统计上共有23个途径被显著富集(p值<0.05,q值<0.05)。三个最显著富集的途径是“抗原加工和呈递”,“细胞粘附分子”和“甲状腺疾病自身免疫”。低表达组没有明显富集的生物学途径。由于CCL5在ccRCC中过表达且与预后不良有关,因此作者接下来进行功能性实验以探讨CCL5的潜在生物学功能。首先,在肾细胞癌769-P细胞系中使用小干扰RNA来敲低CCL5的表达水平,并通过CCK-8评估细胞的增殖能力。结果显示CCL5敲低后细胞系增殖能力降低,同时细胞的侵袭能力也显著下降。
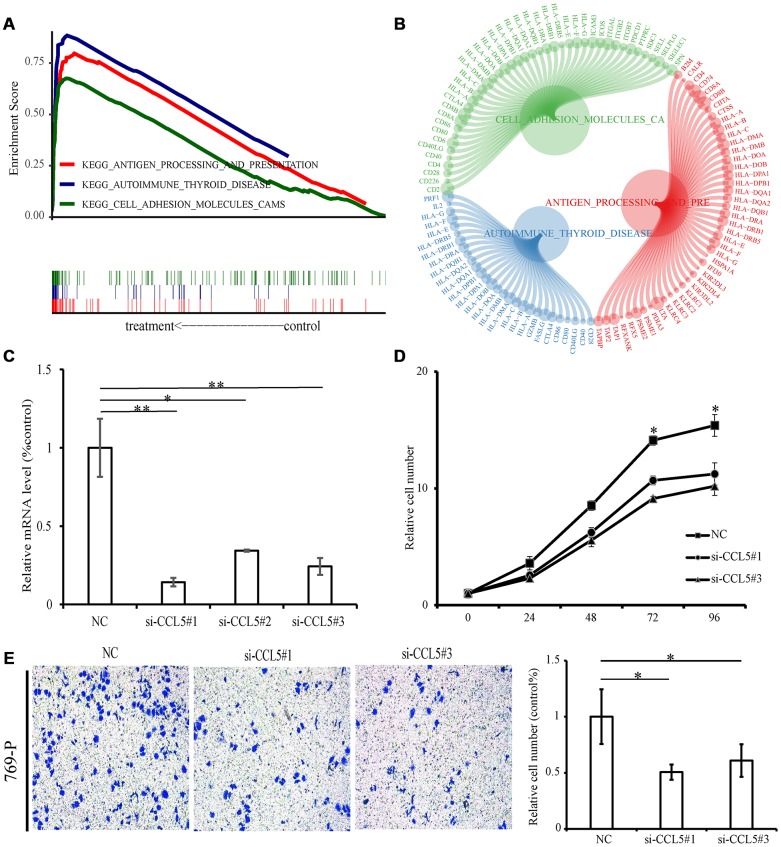
图9GSEA和CCL5实验。(A)GSEA富集分析结果。(B)圆圈图显示了三个富集途径和在富集过程中起作用的核心基因。每个基因对应的圆圈越大,等级度量得分值越大。(C)769-P细胞的正常对照和si-CCL5的相对mRNA水平。(D)CCK-8分析的结果显示,当用si-CCL5处理时,769-P细胞的增殖能力降低。(E)侵袭测定结果显示用si-CCL5处理的769-P细胞的侵袭能力降低。
7、讨论部分:
尽管,目前很多研究通过使用动物肿瘤模型,体外细胞系和临床样品对ccRCC的分子机制探索取得了重大进展。但是,ccRCC微环境的复杂性需要进一步分析和更大的数据集。该研究使用基因表达矩阵构建共表达网络并计算T细胞的浸润水平,并鉴定与CD8 + T细胞最相关的基因。所选模块的基因富集分析表明,它是高度免疫相关的模块。共表达网络和PPI蛋白互作网络中连接度最高的基因挑选为中枢基因(LCK,CD2,CD3D,CD3G,IRF1,IFNG,CCR5,CD8A,CCL5和CXCL9)。在TIMER / TISIDB数据库中查询这10个基因与免疫细胞之间的关系,发现这些基因的表达与免疫细胞(尤其是CD8 + T细胞)呈正相关。进一步,中枢基因和相关的免疫因子,使用TISIDB和STRING数据库构建CD8 + T细胞浸润网络,探索ccRCC免疫机制。TCGA数据集观察所选10个基因的差异表达和临床特征。结果显示肿瘤组织中10个基因的高表达,表明其可能用作生物标志物。与肿瘤分期和分级增加相关的表达对于潜在的预后因素尤其重要。这10个中枢基因可以解释为什么在高度浸润的CD8 + T细胞的情况下ccRCC的预后较差。10个中枢基因Kaplan-Meier生存分析显示,CCL5和IFNG高表达提示临床预后较差。使用Oncomine数据库进行meta分析,癌组织和正常组织之间CCL5表达的差异最大。结合这两项分析,选择CCL5作为检测和预测肾细胞癌预后的最佳潜在生物标志物。
趋化因子配体5(CCL5)属于CC趋化因子家族,其主要作用是与其相应的趋化因子受体结合。几项研究集中于CCL5对肿瘤的作用,发现CCL5可以显着促进肿瘤生长,转移,血管生成和免疫逃逸。CCL5不仅在免疫细胞中表达,而且在肿瘤细胞中表达。乳腺癌细胞中CCL5的表达通过自分泌途径促进乳腺癌细胞的增殖和侵袭。CCL5还促进黑色素瘤和多形性神经胶质瘤的进展。但是,尚无关于CCL5对ccRCC细胞增殖和侵袭作用的实验研究。该研究实验结果表明,si-CCL5可以降低ccRCC细胞的增殖和侵袭能力,表明CCL5可以作为治疗靶点。简而言之,这项研究是首次尝试使用WGCNA和CIBERSORT算法来鉴定ccRCC的潜在CD8 + T细胞相关生物标志物。鉴定了十个hub基因,其在肿瘤中异常高表达并促进肿瘤进展。通过生物信息学和实验的相互验证,CCL5被确定为透明细胞肾细胞癌免疫治疗的潜在生物标志物和靶标。但是,这项研究有一定的局限性。需要更多样本数据来验证这些结果,并且ccRCC中CCL5的具体机制需要进一步研究。
参考文献:
Lin J, Yu M, Xu X, et al. Identification of biomarkers related to CD8+ T cell infiltration with gene co-expression network in clear cell renal cell carcinoma[J]. Aging (Albany NY), 2020, 12(4): 3694.
.png)