8月17日,Cell子刊Molecular Therapy: Nucleic Acid (影响因子5.66)在线发表了美国北卡罗来纳大学教堂山分校Aravind Asokan博士为通讯作者的文章, 介绍他们开发了一种基于腺相关病毒载体(rAAV)的体内表达circRNA并实现翻译蛋白的载体工具[1]。

文章里的AAV表达载体是如何构建的?
载体采用CMV启动子,SV40的PolyA信号序列。分别基于ZKSCAN1和HIPK3基因形成环状RNA 的内含子序列构建circRNA表达体系。为验证所表达的circRNA能够在环化后翻译蛋白,作者利用了拆分的GFP的ORF进行验证(该体系为中科院计算所王泽峰教授团队设计的),只有正确环化的circRNA才能形成完整的GFP的ORF并表达出GFP蛋白。为了排除线性RNA翻译的可能性,作者还构建了线性的RNA对照,即不包含可环化的内含子序列的载体对照。
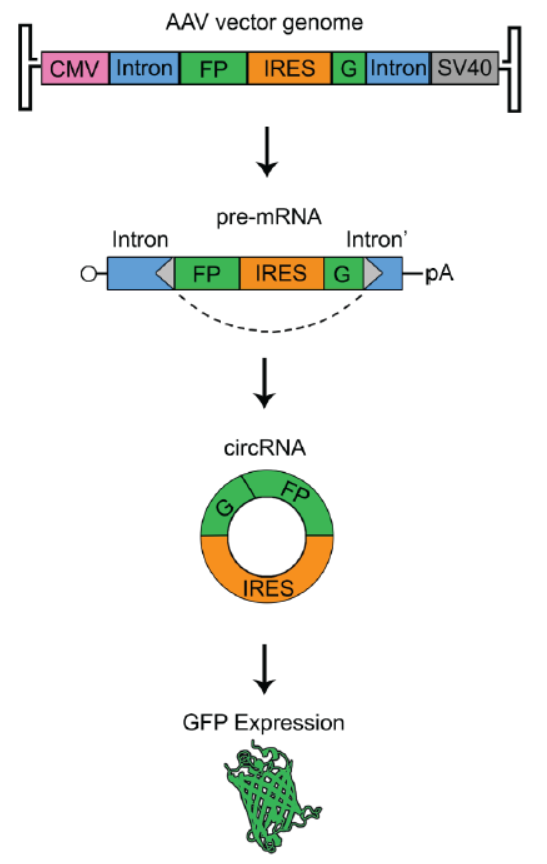
图1 AAV载体框架示意图 (来自[1])
如何证明该载体能特异性表达circRNA并可以正确翻译?
为证明所设计的载体能够正确表达circRNA并能准确翻译蛋白,作者将所构架的载体包装后感染U87细胞,免疫荧光和Western检测证明基于ZKSCAN1和HIPK3基因环化的内含子构建的circRNA过表达载体均能成功表达出GFP蛋白,线性的对照载体几乎没有信号。Northern实验证明了circRNA和前体分子的存在。利用转录抑制剂放线菌素D(Actinomycin D)处理实验证明细胞内circRNA比线性RNA更稳定。
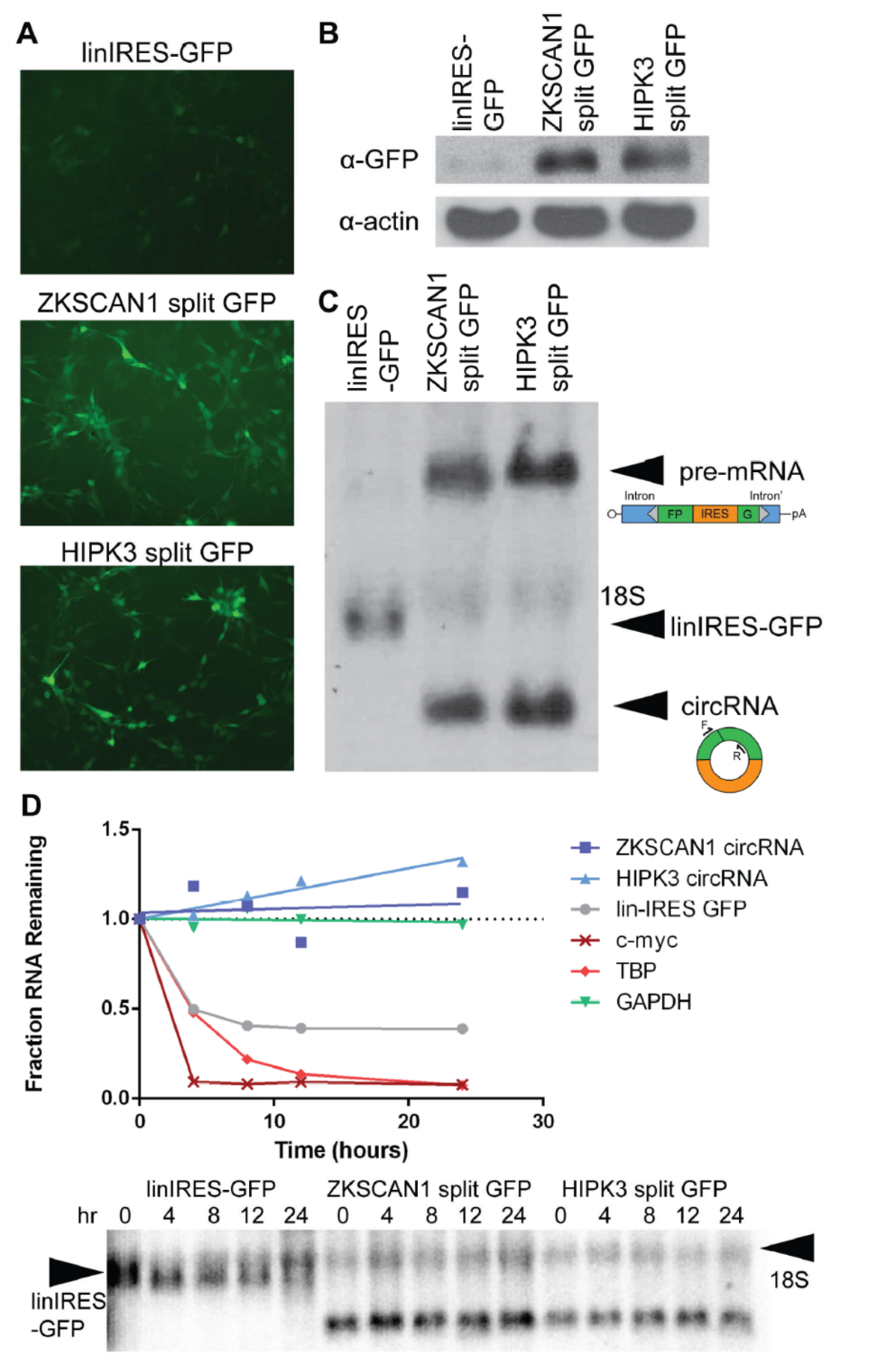
图2 载体表达circRNA并正确翻译蛋白 (来自[1])
体内实验的结果如何?
接下来,作者分别在多种体内组织中验证了所设计的AAV载体注射感染后表达的情况。首先是在心脏组织,将对应序列构建至AAV9载体后包装病毒,静脉注射过了4周之后,心脏组织中可以准确的检测到GFP的表达,对应的线性载体没有表达。
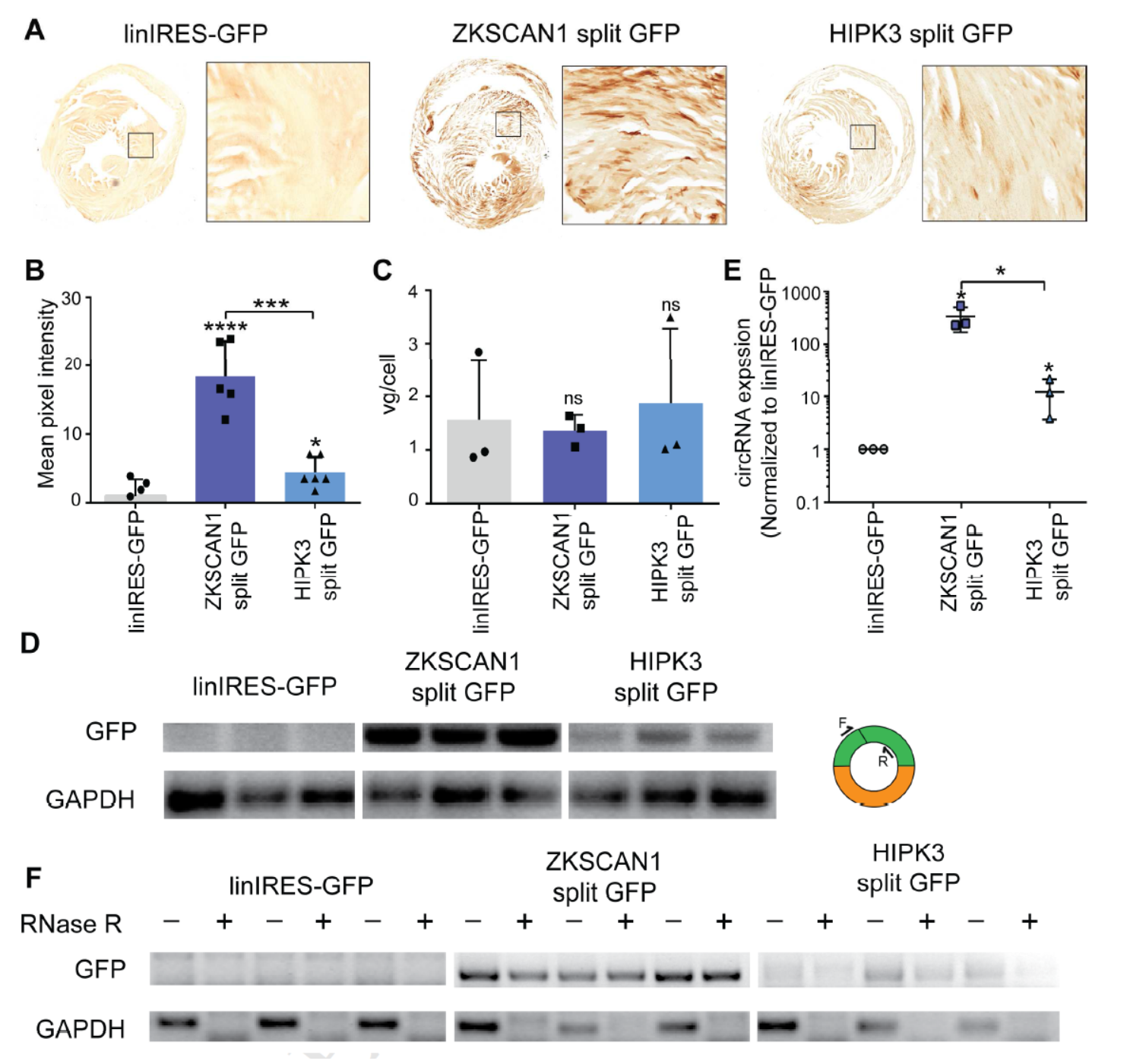
图3 心脏组织可以准确表达circRNA并翻译蛋白 (来自[1])
在肝脏组织中也可以准确表达circRNA并翻译出蛋白。
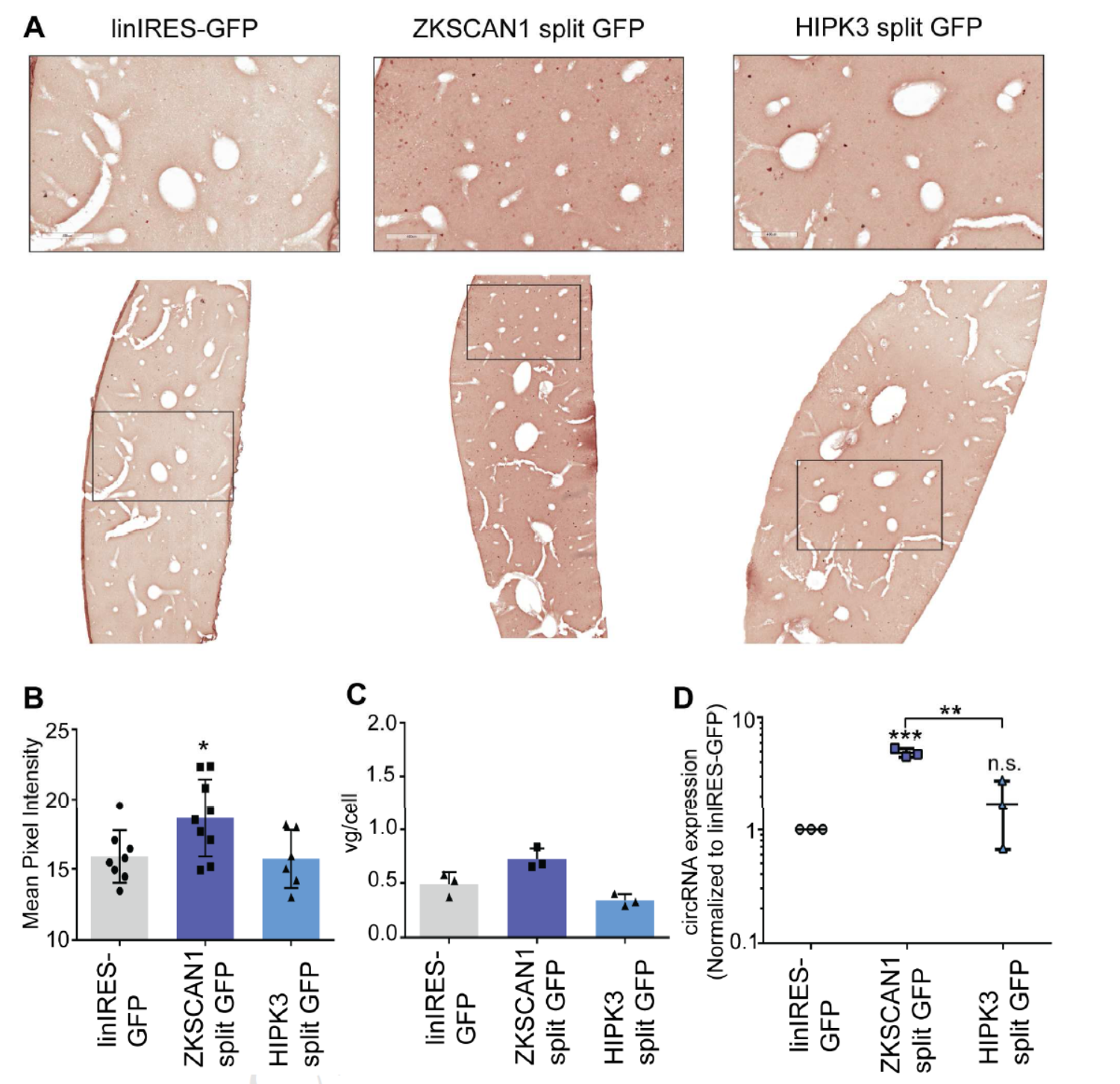
图4 肝组织中可准确表达circRNA并翻译蛋白 (来自[1])
作者也分别在脑组织和眼组织中分析了所构建的AAV载体是否能准确表达circRNA并翻译。在上述的静脉注射模型中,作者在脑组织中发现该体系更容易在星形胶质细胞中表达,偶尔有一些神经元中也可以观察到。当更换为直接脑室注射的模型,观察后表明星形胶质细胞中表达也明显高于其他类型的脑组织细胞。眼球玻璃体内注射AAV病毒后观察,结果表明所构建的载体可以准确的在视网膜截面中表达。
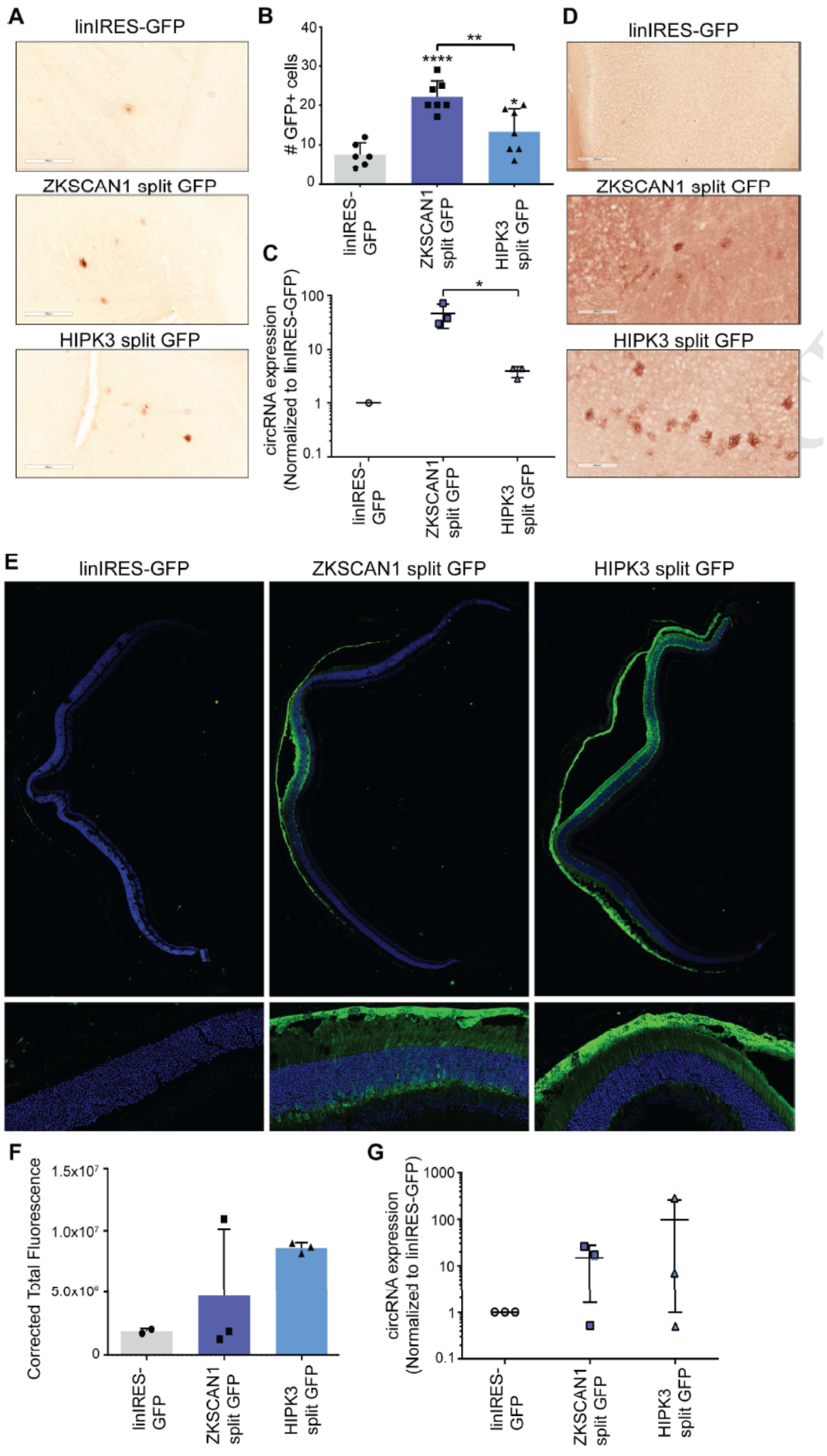
图5 肝组织中可准确表达circRNA并翻译蛋白 (来自[1])
本文的构思比较简单,也证明了基于AAV的体内过表达circRNA并实现翻译蛋白是完全可行的,这一体系对于circRNA研究提供了重要的工具,未来极有可能在circRNA的研究中获得广泛应用。
参考文献:
1. Rita M. Meganck, E.K.B., Ruth M. Castellanos Rivera, Miranda L. Scalabrino, Jeremy E. Wilusz, William F. Marzluff, Aravind Asokan, Tissue-dependent expression and translation of circular RNAs with recombinant AAV vectors in vivo. Molecular Therapy: Nucleic Acid 2018.
.png)
