
朊病毒是基于蛋白质的感染因子,自身可将细胞朊病毒蛋白PrPC催化为其病理异构体PrPSc蛋白。PrPSc在神经组织中的后续聚集和累积会对人类和动物中造成几种常见的致命性神经退行性疾病。外泌体存在于生物液体如血液,尿液和唾液中,如果朊病毒被包装在核内体衍生的被称为外泌体的纳米颗粒中,外泌体可感染受体细胞。自噬是一种基本的胞内降解和循环再生的过程,影响外泌体的形成,但自噬是否调控外泌体中朊病毒的释放尚不清楚。
卡尔加里大学的研究人员,研究了自噬调节对朊蛋白外泌体释放的影响以及这种相互作用如何影响胞内朊病毒的感染。PrPSc蛋白的免疫印迹法,朊病毒转化活性和细胞培养物感染等实验证明,从体外培养的鼠中央神经元细胞(CAD5)和外周神经元细胞(N2a)分离的外泌体含有朊病毒。研究人员发现,利用mTOR抑制剂雷帕霉素刺激自噬后,强烈抑制了外泌体朊病毒的释放。相反,利用wortmannin渥曼青霉素抑制自噬或CRISPR / Cas9介导的自噬蛋白Atg5敲除后,大大增加了外泌体和外泌体相关朊病毒的释放。研究人员还发现,CAD5和N2a神经细胞中exosomal朊病毒释放水平的差异与细胞自噬基础水平的差异有关。综上,这些结果表明自噬调节可以通过干扰其外泌体释放来控制朊病毒的横向转移。研究人员揭示了自噬在朊病毒生命周期中的新作用,这发现可能可以为含有朊病毒的疾病提供有用的靶点。
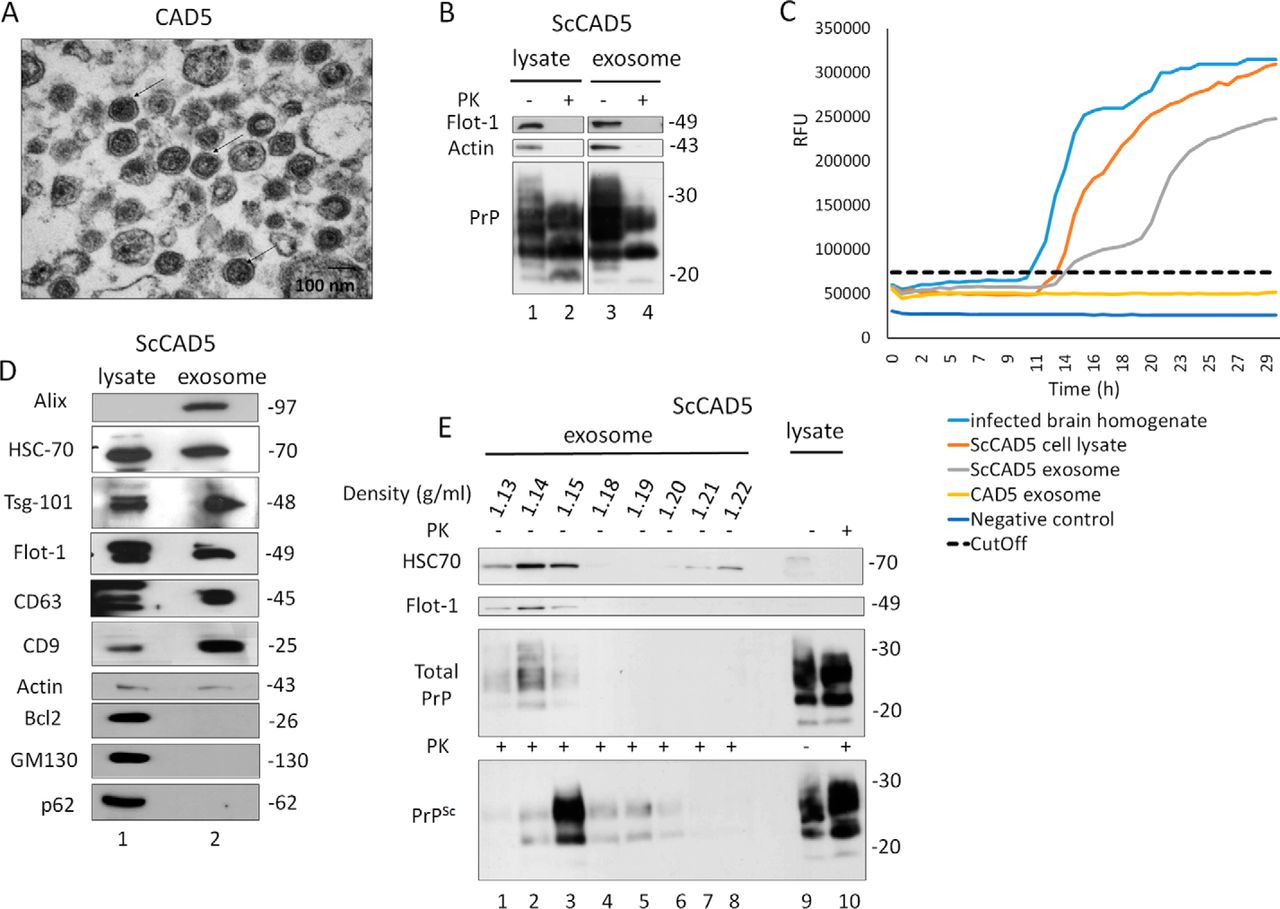
图1 CAD5和N2a神经细胞分泌的外泌体的表型鉴定
A,从CAD5培养基中分离的外泌体电镜形态鉴定;B,ScCAD5细胞裂解物和其来源的外泌体的免疫印迹,检测总PrP(-PK)和PrP Sc (+ PK)(anti-PrP mAb 4H11),PK,蛋白酶K,肌动蛋白Actin被用作上样对照。使用Flotillin-1(Flot-1)作为外泌体的标志物;C,CAD5细胞来源的外泌体,ScCAD5细胞来源的外泌体,ScCAD5细胞裂解物,来自朊病毒病末期小鼠(22L)的10%脑匀浆物或未被感染的组织(阴性对照)的RT-QuIC实验结果。绘制重复孔中硫代黄素-T荧光的平均增加量作为时间的函数。y轴表示RFU,x轴表示时间(h);D, ScCAD5细胞裂解物和从ScCAD5培养基分离的外泌体的免疫印迹分析。外来体样品对外来体标志物Alix,HSC70,Tsg-101,flotillin-1,CD63和CD9呈阳性,对线粒体标志物Bcl2,高尔基体标志物GM130和核标志物核孔蛋白p62呈阴性。肌动蛋白Actin被用于上样对照; E,将ScCAD5外泌体沉淀加载在连续蔗糖梯度的顶部并超速离心。通过Western印迹分析不同组分中HSC70,flotillin-1和mAb 4H11的表达情况,以检测PrP / PrPSc。泳道9和10分别表示PK消化之前和之后的细胞裂解物
参考文献
1. Abdulrahman BA, Abdelaziz DH, Schatzl HM. (2018) Autophagy regulates exosomal release of prions in neuronal cells. J Biol Chem 293(23):8956-8968. DOI:10.1074/jbc.RA117.000713.
2. 信息来源:https://www.exosome-rna.com/autophagy-regulates-exosomal-release-of-prions-in-neuronal-cells/
.png)
