环状RNAs(CircRNAs)是一类由前体mRNA反向剪接产生的闭环RNAs,具有细胞类型特异性、组织特异性和发育阶段特异性等表达模式。CircRNA既没有5’帽也没有3’尾,表现出抗RNase R的特性。CircRNA主要通过与miRNA或蛋白质相互作用,也可以进行独立翻译。大量研究发现,circRNAs在包括癌症在内的许多人类疾病中发挥调节作用。
液-液相分离(LLPS)指的是一种细胞内不同成分(大分子蛋白质,RNA,DNA)间相互碰撞、融合形成液滴,从而使一些成分被包裹在液滴内,一些成分被阻隔在液滴外的现象。促进蛋白质间相互作用的蛋白结合区域,以及内在无序区域均可以触发LLPS。SGs是无细胞质膜核糖核蛋白(RNP)缩合物,在热休克、氧化应激、渗透应激或营养缺乏等各种环境应激下形成[1]。
近日,中国科学院北京生命科学研究院赵方庆团队在Advanced Science在线发表了题为circVAMP3 Drives CAPRIN1 Phase Separation and Inhibits Hepatocellular Carcinoma by Suppressing c-Myc Translation的文章。研究发现circVAMP3在体内外对HCC细胞的增殖和转移进行负性调节,从而通过抑制c-Myc翻译下调Myc原癌基因蛋白的蛋白水平。CircVAMP3是肝癌的一个潜在预后指标,可能作为肝癌治疗的一个靶点。

作者从20对HCC组织和临近正常组织中筛选出17个差异表达的circRNAs,从中选择了明显下调的circVAMP3进行进一步的功能研究。如图1c所示,CircVAMP3在人肝癌细胞中主要分布在细胞质。临床样本分析发现,与相邻正常组织相比,circVAMP3在肿瘤组织中显著下调。CircVAMP3的表达与肿瘤大小呈负相关,较低的circVAMP3水平分别表现为肿瘤晚期和肿瘤血管浸润。进一步细胞功能实验发现,circVAMP3抑制SMMC-7721细胞的增殖、生长和转移。
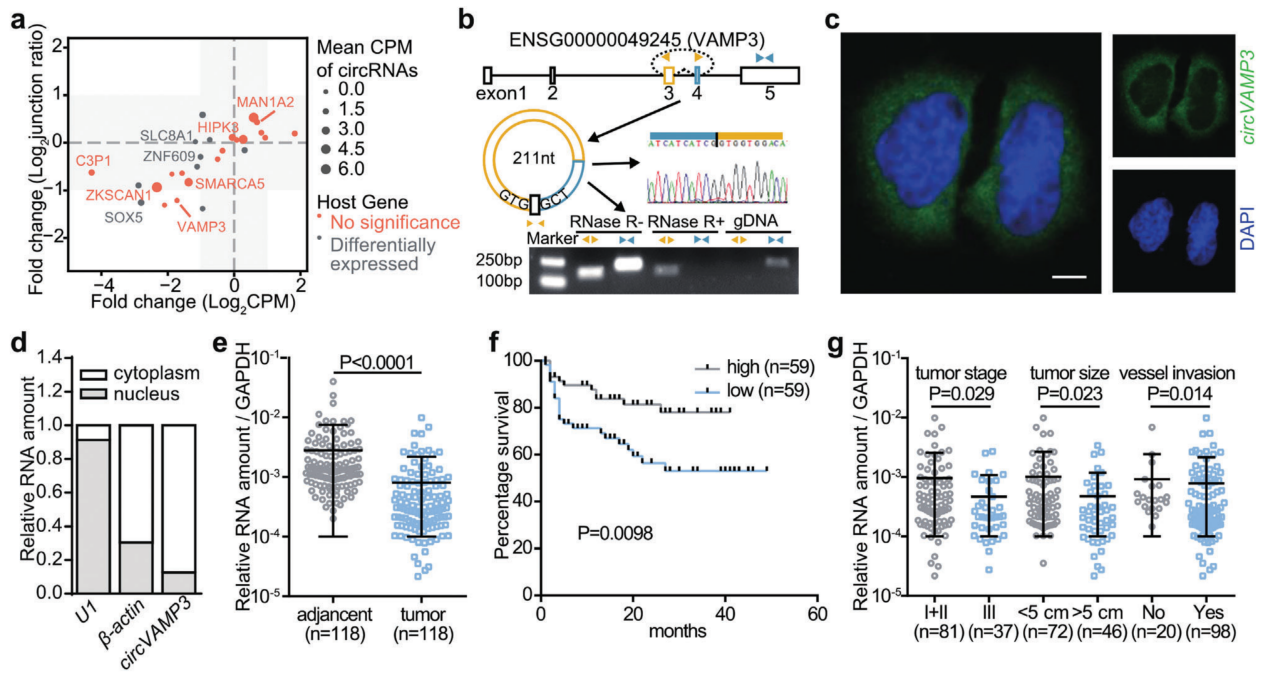
图1. circVAMP3在HCC中降低并与患者预后负相关
体外细胞功能实验发现,circVAMP3抑制SMMC-7721细胞的增殖、生长和转移。已有研究发现circRNAs通过miRNA Sponge机制在肝癌中发挥作用,而有关环状RNAs在HCC进展中的蛋白结合作用需要进一步研究[2]。通过RNA pull-down及质谱实验,检测肝癌细胞中与circVAMP3结合的蛋白质。如图2所示,在共同富集的5个蛋白中,只有CAPRIN1可以被SMMC-7721和Huh7细胞的circVAMP3探针高度富集。随后,筛选验证了CAPRIN1的相互作用蛋白G3BP1。
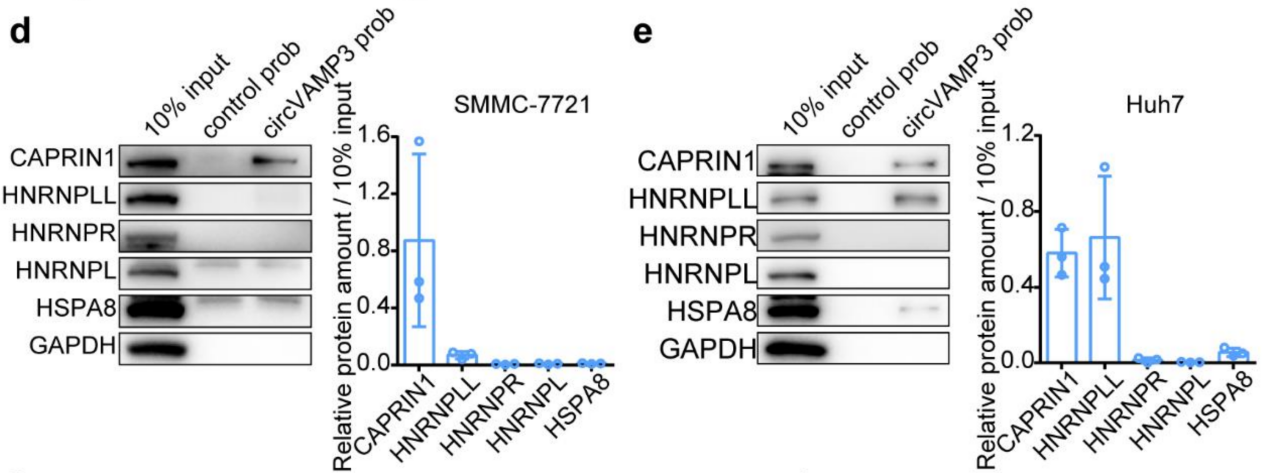
图2. 肝癌细胞RNA pull-down产物Western Blot分析
作者通过FISH-IF共定位发现,circVAMP3、CAPRIN1和G3BP1定位于细胞质并共定位于凝析物中。随后,作者使用FRAP和荧光定位实验发现CAPRIN1和G3BP1在体外和体内都可以组装成液体样颗粒,而circVAMP3在颗粒中共定位。
CAPRIN1蛋白通过其保守的RGG结构域与circVAMP3产生多个结合位点,这表明circVAMP3可以通过支撑CAPRIN1蛋白促进LLPS。由于circVAMP3不直接与G3BP1相互作用,因此circVAMP3不能促进G3BP1的体外LLPS。考虑到G3BP1可以与CAPRIN1相互作用形成蛋白复合物,circVAMP3可能通过与CAPRIN1相互作用来支架和浓缩CAPRIN1-G3BP1复合物,从而触发LLPS。如图3所示,作者通过IF及体外LLPS实验发现,circVAMP3触发CAPRIN1的相分离,促进应力颗粒的形成。
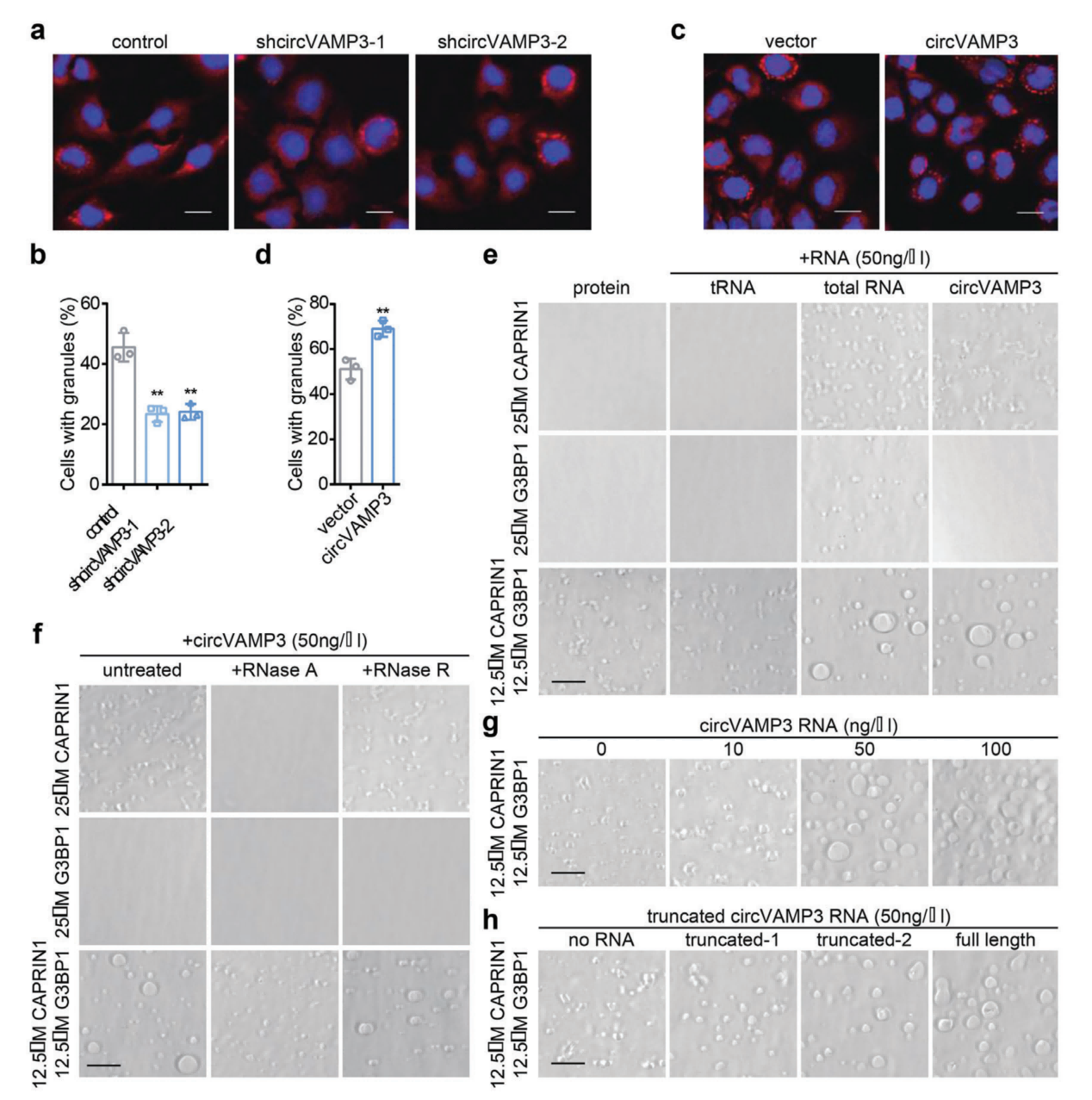 图3. circVAMP3促进LLPS
图3. circVAMP3促进LLPS
考虑到circVAMP3对SGs诱导的作用,作者假设circVAMP3可能通过颗粒在HCC中发挥抑癌作用。通过KEGG对20对HCC及邻近组织中差异表达基因进行通路分析,发现细胞周期进展显著增强。为了探索circVAMP3在细胞周期进展中的作用,作者验证发现c-MYC蛋白在circVAMP3沉默的SMMC-7721细胞中表达上调,在circVAMP3过表达的SMMC-7721细胞中表达下调。而c-Myc mRNA表达水平在circVAMP3沉默的SMMC-7721细胞中无显著变化,在circVAMP3过表达SMMC-7721细胞中上调。结果表明,c-MYC蛋白的差异表达并不是因为circVAMP3对c-MYC基因表达的影响。c-MYC和CAPRIN1的免疫荧光分析显示,c-MYC蛋白未在SGs中共定位。c-Myc的RNA FISH结合CAPRIN1和G3BP1的免疫荧光显示,c-Myc RNA、CAPRIN1和G3BP1在SGs中共定位。
已有研究发现CAPRIN1的相分离可能调控mRNA的翻译[3]。因此,circVAMP3可能通过调控c-MYC翻译来影响c-MYC蛋白的表达水平。
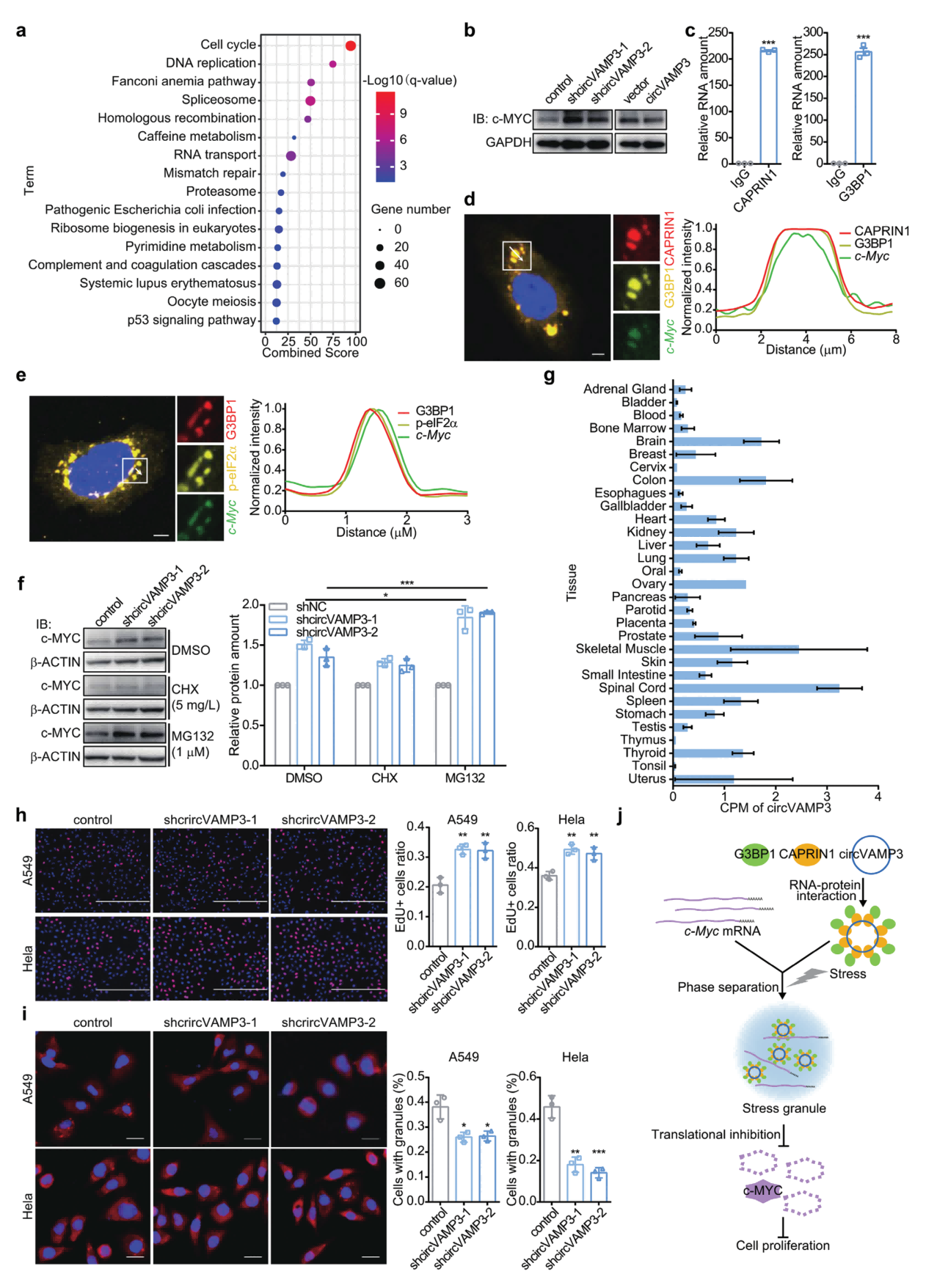 图4. circVAMP3抑制c-Myc的翻译,并在其他癌症中发挥其肿瘤抑制功能
图4. circVAMP3抑制c-Myc的翻译,并在其他癌症中发挥其肿瘤抑制功能
如图4j所示,G3BP1与CAPRIN1相互作用形成蛋白复合物,circVAMP3通过与CAPRIN1相互作用来支架和浓缩CAPRIN1-G3BP1复合物,从而触发LLPS。由于circVAMP3和VAMP3线性转录本具有相同的序列(外显子3和外显子4),VAMP3 RNA也可能具有驱动LLPS的潜力。然而,circVAMP3比VAMP3 liner transcripts更稳定(图1b),这显示了其在促进LLPS方面的优势。
总之,本研究鉴定了一种重要的环状RNA,circVAMP3,它可以与CAPRIN1物理相互作用,促进SGs的形成并抑制c-Myc的翻译。鉴于circVAMP3在人体各种组织中含量丰富,并在相应的肿瘤组织中表达下调,它可能成为肝癌等多种癌症的新的诊断和治疗靶点。
原文链接:https://onlinelibrary.wiley.com/doi/epdf/10.1002/advs.202103817
参考文献:
- Aulas, M. M. Fay, S. M. Lyons, C. A. Achorn, N. Kedersha, P. Anderson, P. Ivanov, J. Cell Sci. 2017, 130, 927.
- W. Du, W. Yang, E. Liu, Z. Yang, P. Dhaliwal, B. B. Yang, Nucleic Acids Res. 2016, 44, 2846.
- Wang, L. Cao, R. F. Thorne, X. D. Zhang, J. Li, F. Shao, L. Zhang,M. Wu, Sci. Adv. 2021, 7, eabe5708.



 图3. circVAMP3促进LLPS
图3. circVAMP3促进LLPS 图4. circVAMP3抑制c-Myc的翻译,并在其他癌症中发挥其肿瘤抑制功能
图4. circVAMP3抑制c-Myc的翻译,并在其他癌症中发挥其肿瘤抑制功能.png)