抗癌治疗的最新进展促使癌症幸存者的数量稳步增加,矛盾的是,也增加了心力衰竭(HF)患者的数量,这些抗肿瘤治疗产生了不好的心脏毒性等副作用。减少或逆转化疗诱导的心力衰竭的治疗方案未能取得较好的效果。环状RNA因其特殊的闭环结构而具有较高的稳定性,因此具有较高的药物开发潜力。
2022年6月27日,汉诺威医学院Thomas Thum和Christian Bär作为共同通讯在European Heart Journal (IF 35.855)发表文章《A circular RNA derived from the insulin receptor locus protects against doxorubicin-induced cardiotoxicity》。他们指出:在临床前小鼠和人类模型中,Circ-INSR超表达可预防阿霉素诱导的心功能障碍。此外,体外制备的Circ-INSR模拟物减少了阿霉素应激下的心肌细胞死亡,突出了基于Circ-INSR的RNA治疗在未来临床应用中的潜力[1]。

Nature Reviews Cardiology杂志主编Gregory B Lim
2022年7月22日,Nature Reviews Cardiology杂志主编Gregory B Lim对上述的Circ-INSR相关研究发表评论性文章《Circular RNA prevents doxorubicin-induced cardiotoxicity》。基于体外人工制备的circRNA mimics拥有巨大的Translational perspective,Gregory Lim主编根据Original article两位一作Dongchao Lu和Shambhabi Chatterjee的论述,探讨分析了从编码胰岛素受体基因衍生的环状RNA(Circ-INSR)的过度表达可防止因使用阿霉素进行抗癌治疗而发生心脏功能障碍的发展。Circ-INSR是一种新的、丰富的、高度保守的环状RNA,具有良好的治疗潜力。

TALK
“环状RNA是一种独特的非编码RNA亚型,主要来源于具有共价闭合结构的前体mRNA。”
“在我们之前的工作中,我们阐明了在阿霉素诱导的心力衰竭背景下CircRNA的形成[2]。”
在这项工作的基础上,Lu、Chatterjee及其同事筛选了新的环状RNA,并确定Circ-INSR是在阿霉素诱导的心脏毒性应激下心肌细胞活力的重要调节因子。在啮齿动物和接受阿霉素治疗的患者中,Circ-INSR下调,导致心肌细胞死亡和心功能不全。
在体外和阿霉素慢性心脏毒性小鼠模型中,基于腺相关病毒的Circ-INSR超表达可预防阿霉素诱导的啮齿动物和人心肌细胞心脏毒性。同样,在体外转录和环化的Circ-INSR模拟物也能抵抗阿霉素诱导的心脏毒性。
研究人员发现,Circ-INSR的表达受Brca1基因的调节,并且Circ-INSR与SSBP1蛋白发生物理相互作用,并调节心肌细胞中的凋亡和代谢途径。
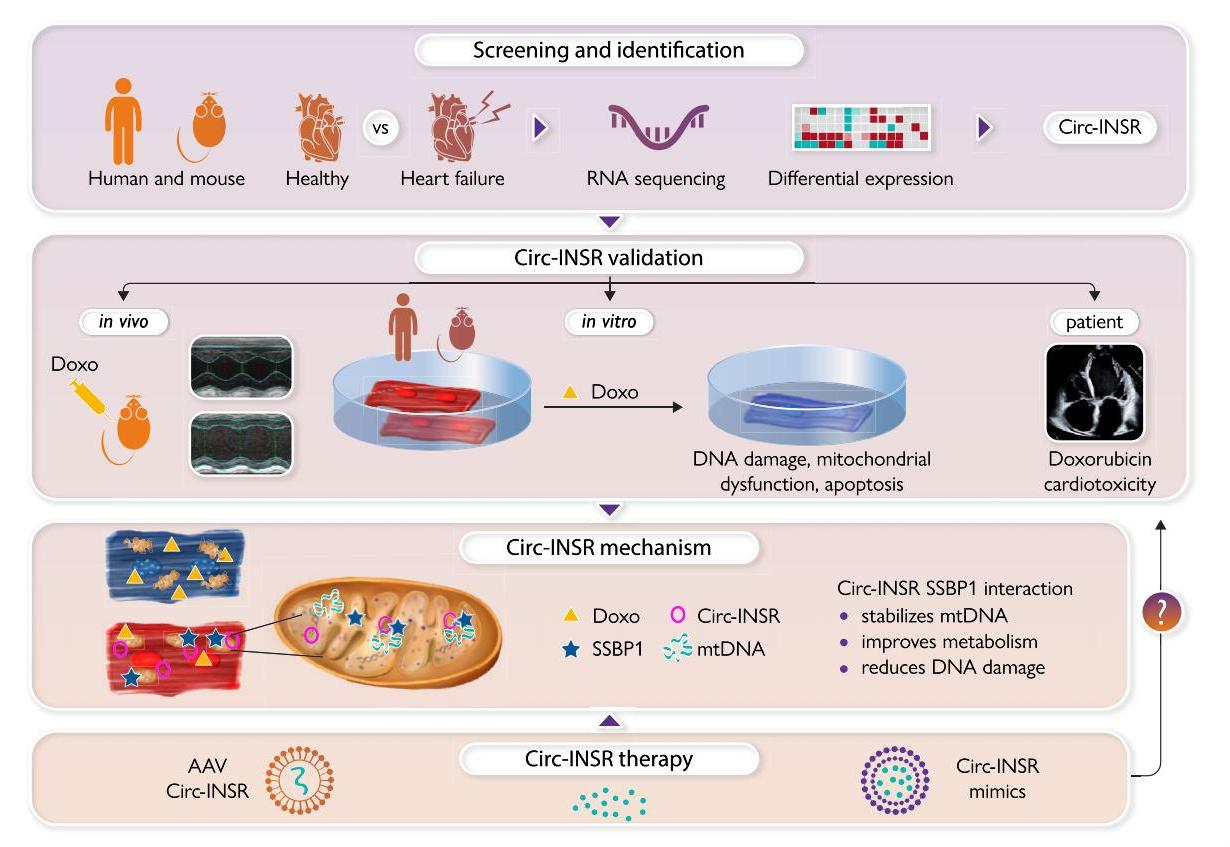
环状RNA疗法对心衰的保护作用
TALK
“体外转录的环状RNA的纯度和免疫原性需要进一步研究。”
“此外,需要开发新的心脏特异性传递这些circRNA模拟物的方法。”
同时,鉴于RNA疫苗的出现和环状RNA的高稳定性(能够抵抗核外降解),Lu和Chatterjee对基于circRNA的治疗的翻译潜力充满信心。
[2]. Viereck J, Buhrke A, Foinquinos A, Chatterjee S, Kleeberger JA, Xiao K, et al. Targeting muscle-enriched long non-coding RNA H19 reverses pathological cardiac hypertrophy. Eur Heart J 2020;41:3462–3474
.png)
