人类对于扼制COVID-19已经开展了行动。目前,已有几种药物用于COVID-19的临床治疗,如小分子抗体、中和抗体和单克隆抗体等;腺病毒载体疫苗、灭活疫苗、重组亚单位疫苗和核酸疫苗也在加速研发和实验中。然而,疫苗疗效的稳定和不良反应因人而异。因此,开发安全有效的药物和疫苗来预防、诊断和治疗COVID-19刻不容缓。

一、认识SARS-CoV-2与其相关的circRNA
SARS-CoV-2进入细胞后,借助宿主细胞的内源性转录机制和自身特性在宿主内复制和传播,诱导细胞快速衰变。为什么SARS-CoV-2不能够被快速识别和消灭呢?主要因为SARS-CoV-2可抑制MHCI类通路的激活,而该通路在抗病毒免疫过程中有着关键的作用(如图1)。此外,SARS-CoV-2不仅直接损害肺组织,还触发细胞内环境“风暴”—过度活化细胞因子和免疫细胞,导致弥漫性肺泡损伤,加剧患者呼吸衰竭,甚至可能导致无法控制的系统性炎症反应。
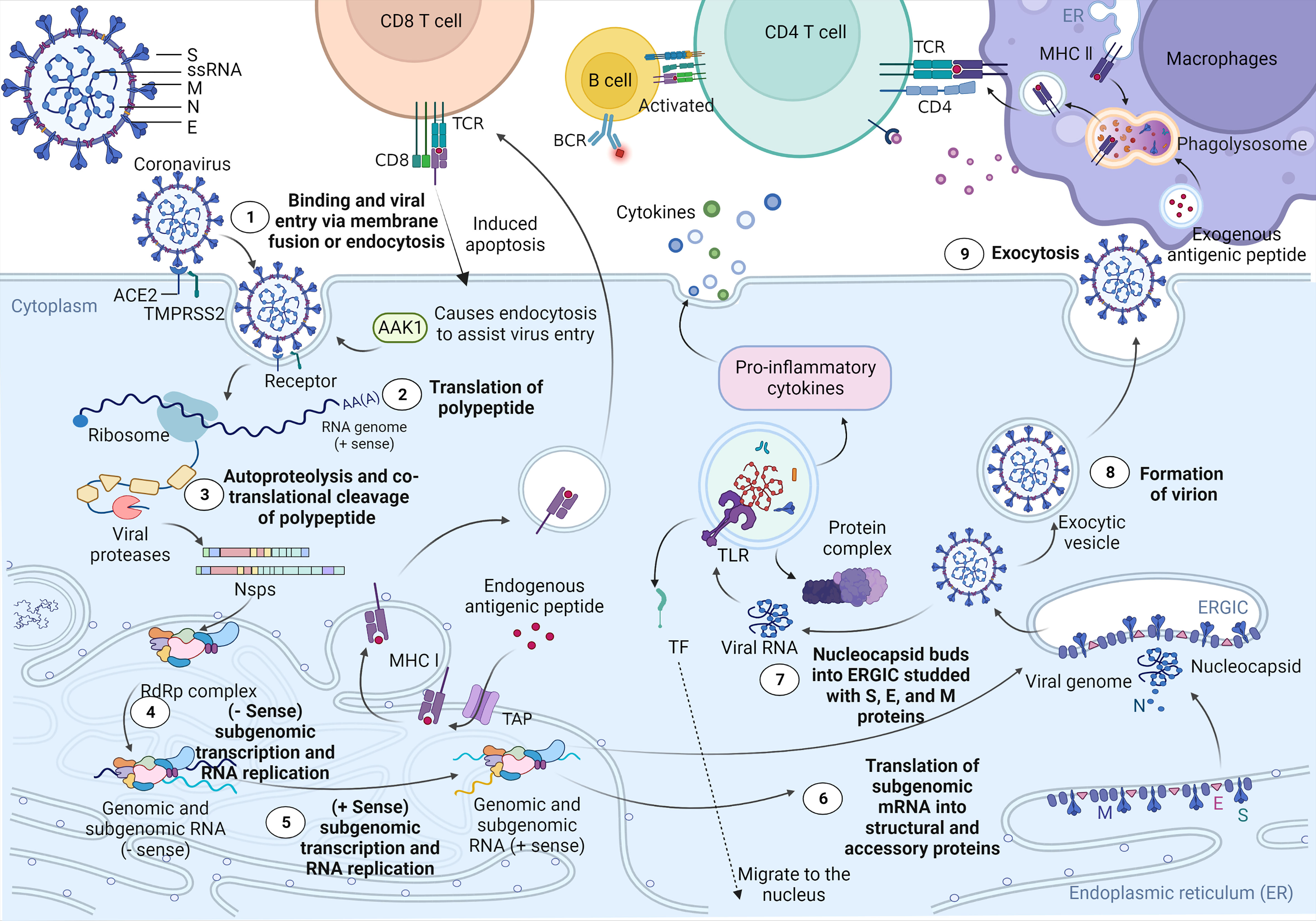
图1.SARS-CoV-2进入细胞的机制和生命周期
二、潜藏于SARS-COV-2感染后的circRNA机制
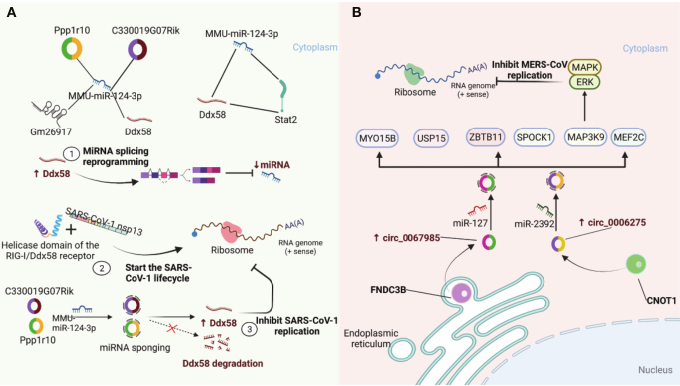
图2.circRNA作为miRNA海绵影响病毒复制
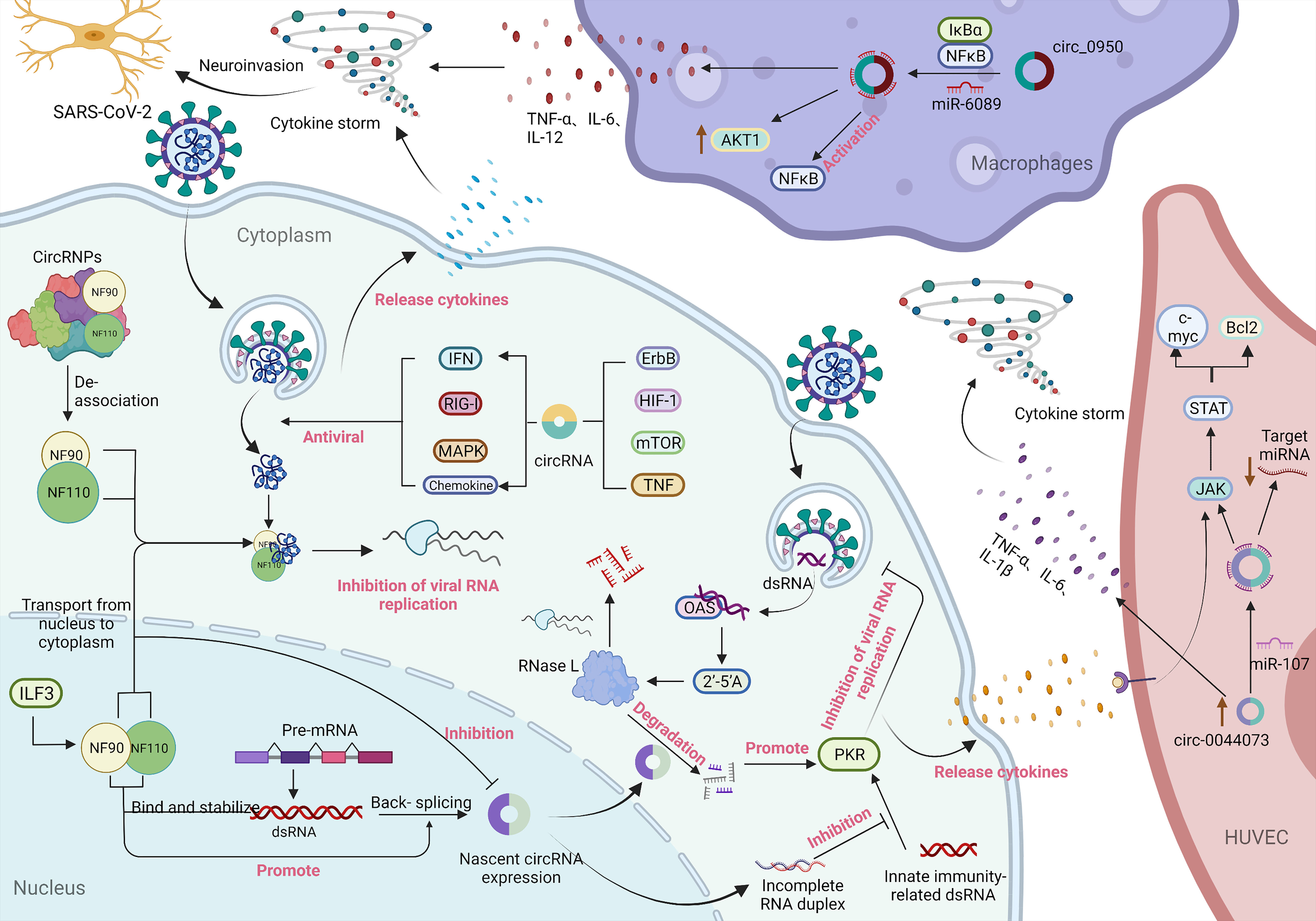
图3.SARS-CoV-2感染中的circRNA在炎症反应中的潜在机制
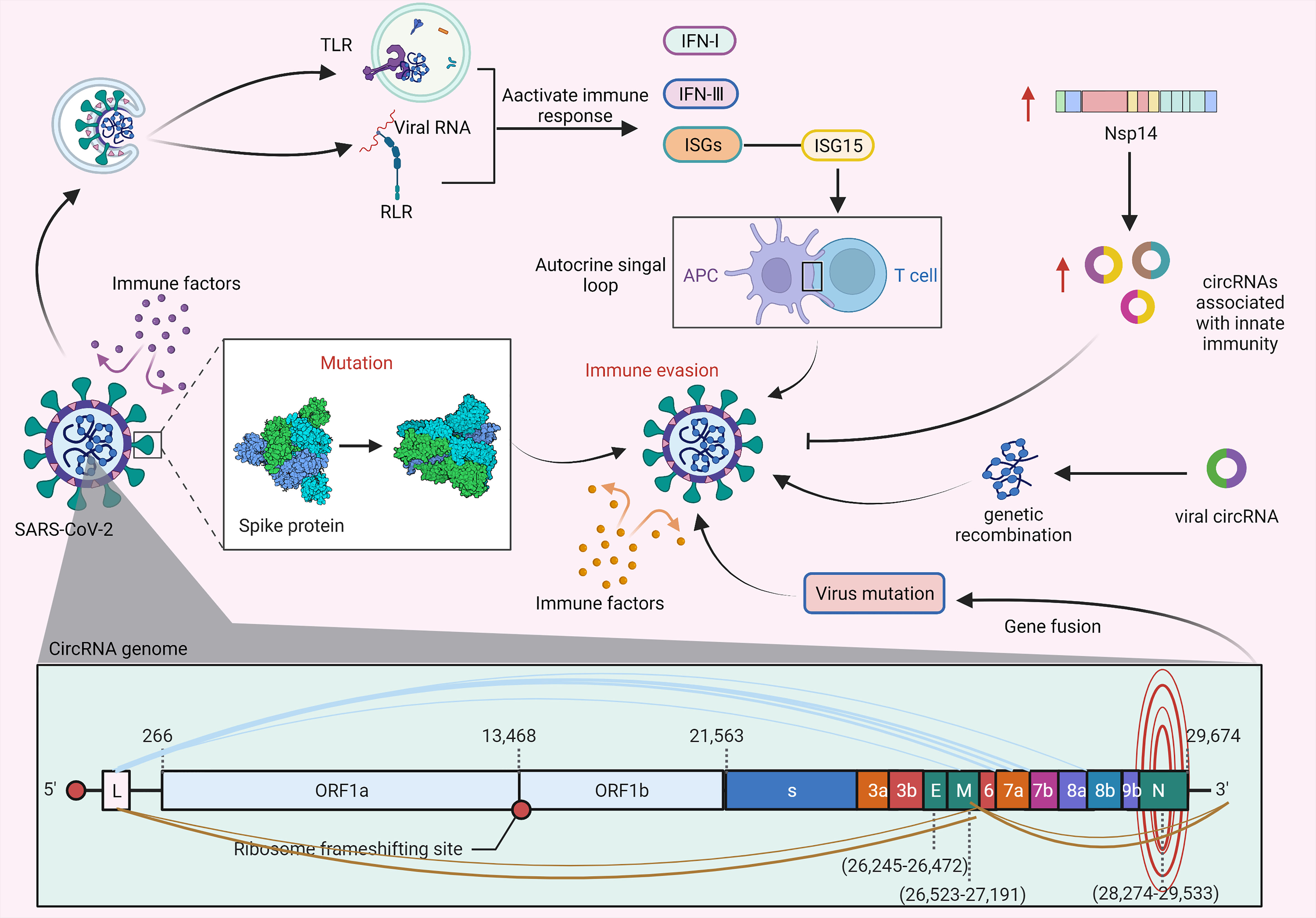
图4.circRNA调节SARS-CoV-2的免疫逃避
三、COVID-19新疗法-circRNA的应用
circRNA抗RNase R降解,半衰期较长,表达模式受病毒感染影响,在COVID-19患者的循环系统中含量丰富并具有独特的功能。外泌体可反映细胞的病理状态,它们可以用作各种疾病的诊断标记。而最近的研究表明外泌体circRNA可能是COVID-19复发的一个关键因素。因此,外泌体相关环状RNA的鉴定和分离可能有助于COVID-19的诊断。
病毒感染引起的免疫可以保护细胞功能,抵抗病毒入侵,清除病毒,清除感染。然而,过度激活免疫反应可能会对宿主造成严重的损伤。COVID-19患者中SARS-CoV-2可诱发免疫风暴,从而对组织和器官造成广泛损伤。而circRNA-miRNA-mRNA调控网络有助于调控免疫相关因子及其涉及的信号通路(NF-kB/MAPK/mTOR)降低免疫风暴,可能成为治疗COVID-19的新途径。
国外以Orna Therapeutics和Laronde为代表,国内环码生物、圆因生物、吉赛生物和科锐迈德等公司先后布局环形RNA技术平台。目前尚未有基于circRNA的产业级癌症疫苗被开发出来,因此需要进一步探究circRNA疫苗在肿瘤免疫治疗中的适用性。我们期待这一创新技术能够早日进入临床开发阶段,展现它在感染性疾病、自身免疫病、罕见病以及癌症的预防或治疗的潜力。
https://doi.org/10.3389/fimmu.2022.980231
参考文献:
[1] Aleem A, Akbar Samad AB, Slenker AK. Emerging variants of SARS-CoV-2 and novel therapeutics against coronavirus (COVID-19). StatPearls. Treasure Island (FL: StatPearls Publishing Copyright © 2022, StatPearls Publishing LLC (2022).
[2] Torjesen I. Covid-19: Delta variant is now UK’s most dominant strain and spreading through schools. BMJ (Clin Res ed) (2021) 373:n1445. doi: 10.1136/bmj.n1445
[3] Awan FM, Yang BB, Naz A, Hanif A, Ikram A, Obaid A. The emerging role and significance of circular RNAs in viral infections and antiviral immune responses: possible implication as theranostic agents. RNA Biol (2021) 18(1):1–15. doi: 10.1080/15476286.2020.1790198
[4] Zhou Z, Sun B, Huang S, Zhao L. Roles of circular RNAs in immune regulation and autoimmune diseases. Cell Death Dis (2019) 10(7):503. doi: 10.1038/s41419-019-1744-5
转载请联系邮箱授权:circRNA@163.com
.png)
