
接下来,作者评估了circBtnl1在ISCs中的功能。敲低circBtnl1显著破坏了小肠和结肠的类器官形成能力。FISH检测了circBtnl1在小鼠各组织中的表达,作者发现circBtnl1在各组织中广泛表达,其中小肠、结肠和胃是高表达的前三个组织;并且circBtnl1仅定位于肠隐窝和小肠类器官的细胞质中,核-细胞质分离实验也验证了这一结果。这些结果表明circBtnl1在小鼠ISCs中高表达。
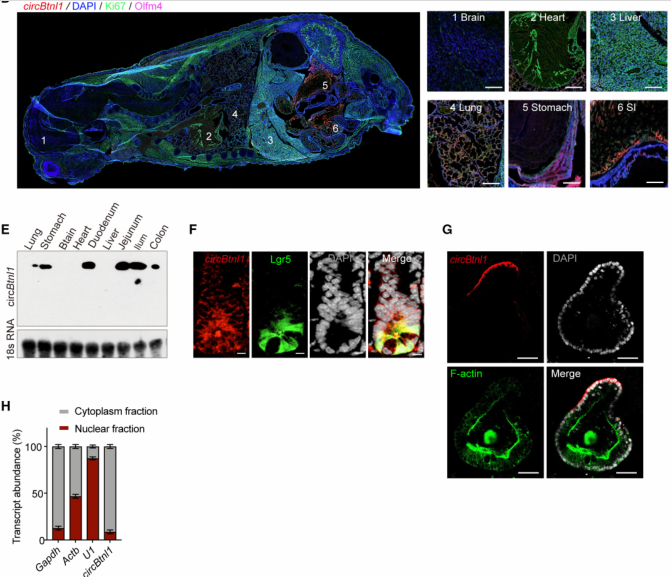
图1. circBtnl1在ISCs中高表达
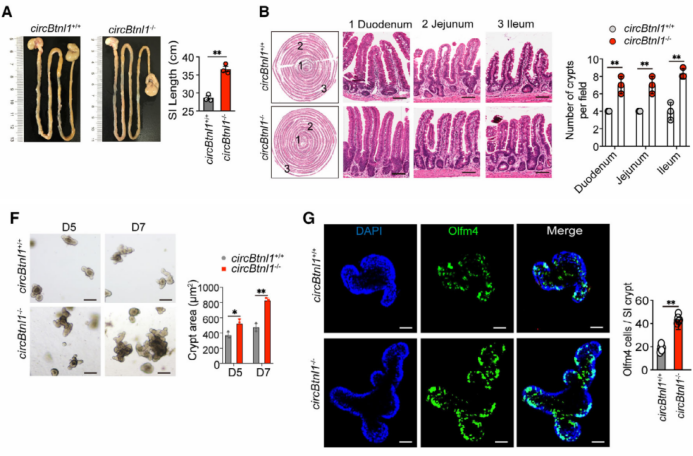
图2. circBtnl1基因敲除促进了ISCs的自我更新
作者发现,过表达Ddx3y显著促进了组织腔形成能力。而circbtnl1则逆转Ddx3y过表达在类器官中的作用。Ki67染色检测小肠类器官的结果与上述结果一致。此外,circBtnl1在类器官形成和增殖中的作用可以受Ddx3y反向调控,这表明circBtnl1在ISCs中通过Ddx3y发挥作用。
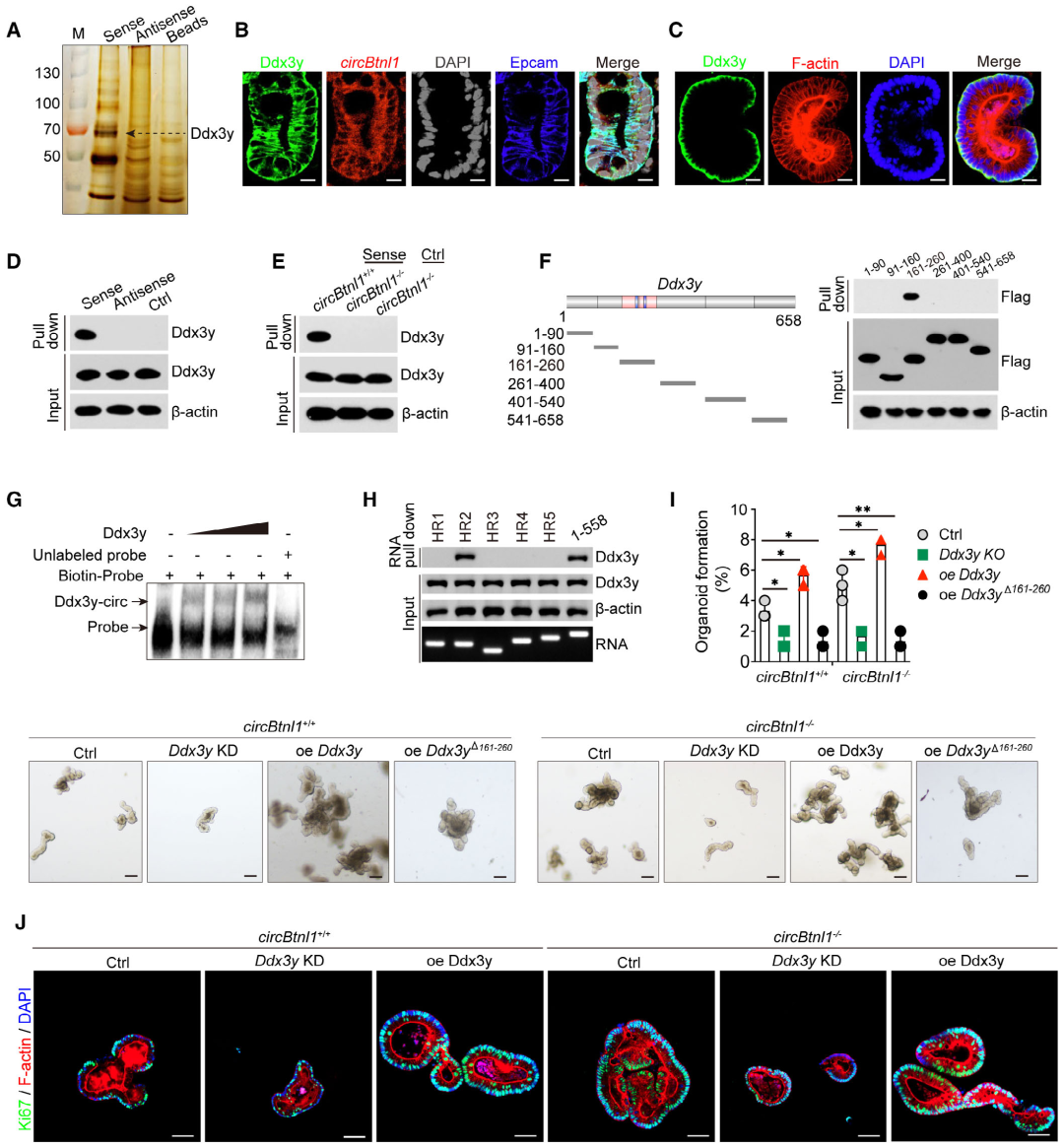
图3. CircBtnl1在ISCs中与Ddx3y结合
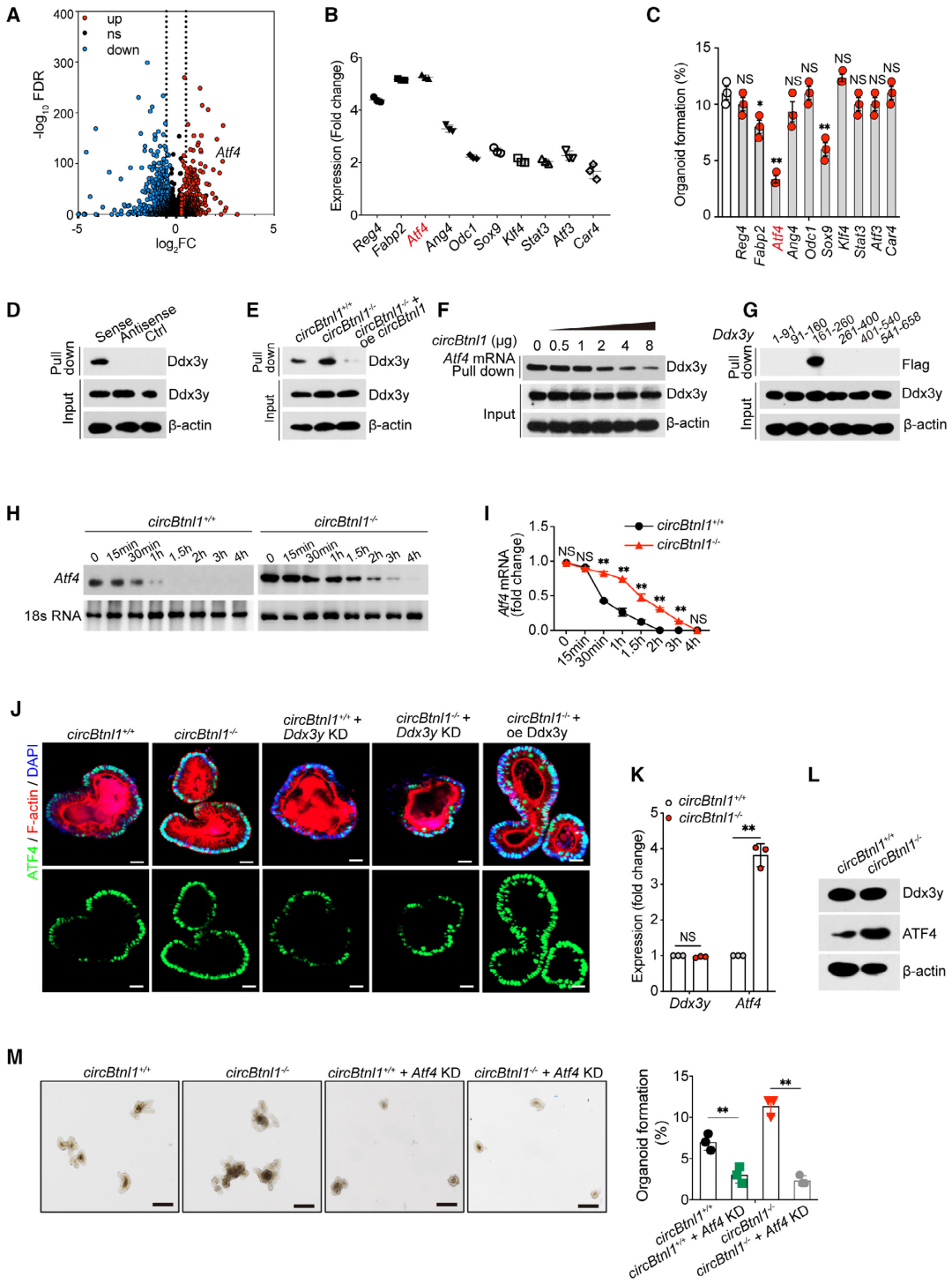
图4. CircBtnl1和Atf4 mRNA竞争性结合Ddx3y,调节Atf4 mRNA的稳定性
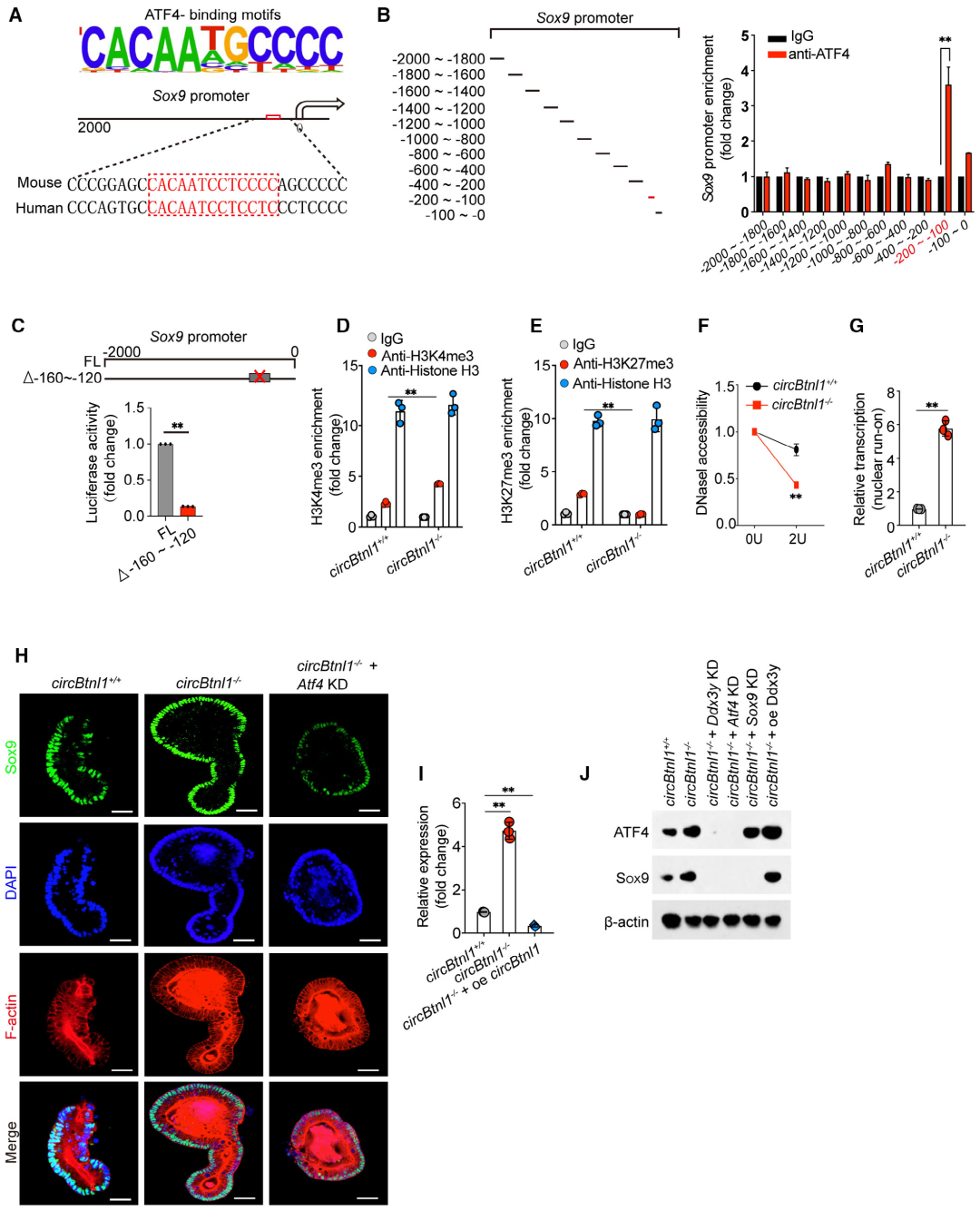
图5. CircBtnl1敲除可促进ATF4进入Sox9启动子,触发其转录
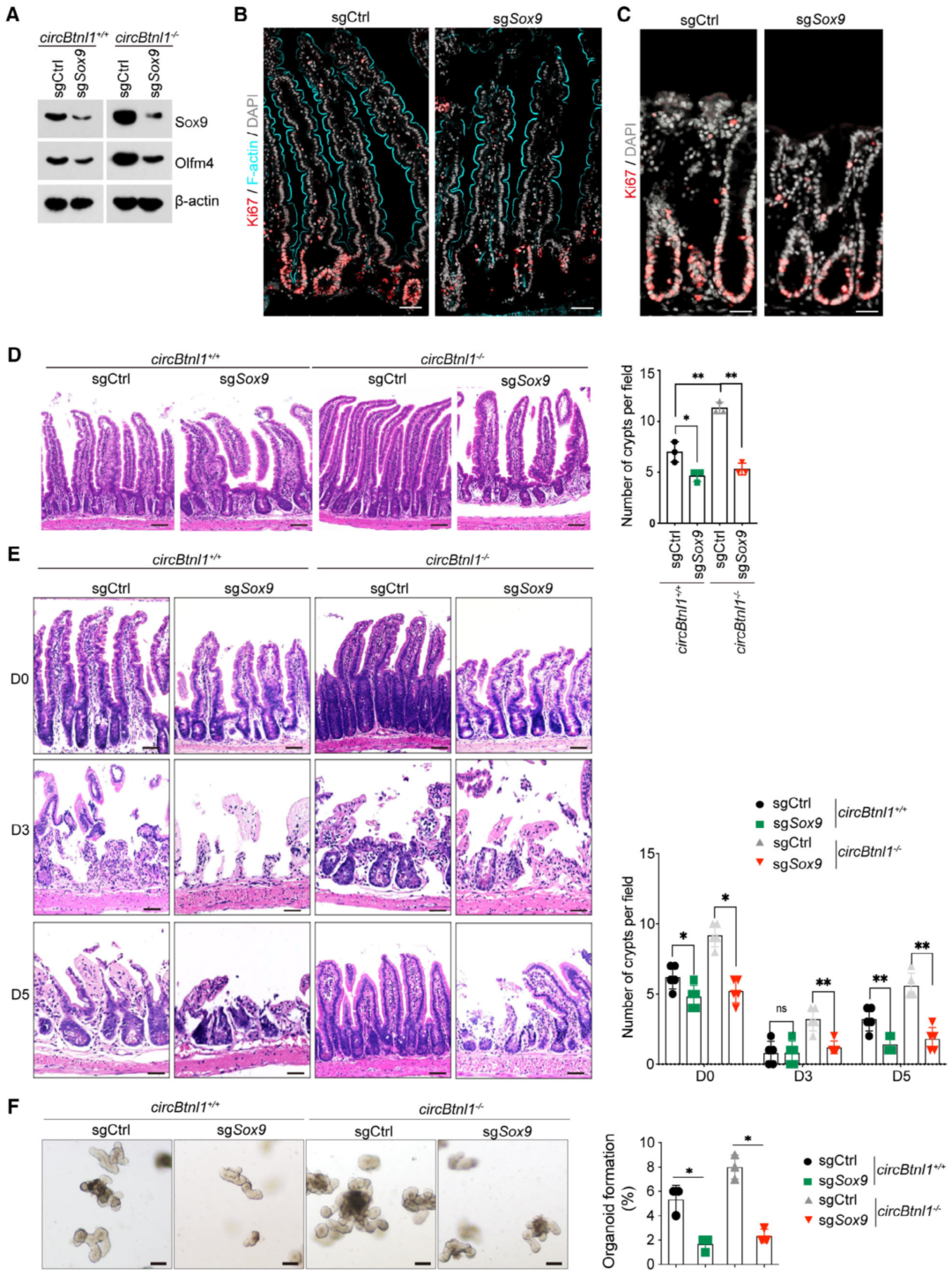
图6. Sox9基因敲除会损害ISCs的自我更新
参考文献:
[1] Yan KS, Janda CY, Chang J, Zheng GXY, Larkin KA, Luca VC, Chia LA, Mah AT, Han A, Terry JM et al (2017) Non-equivalence of Wnt and R-spondin ligands during Lgr5(+) intestinal stem-cell self-renewal. Nature 545:238–242
[2] Vo JN, Cieslik M, Zhang Y, Shukla S, Xiao L, Zhang Y, Wu YM, Dhanasekaran SM, Engelke CG, Cao X et al (2019) The landscape of circular RNA in cancer. Cell 176: 869–881.e13
转载请联系邮箱授权:circRNA@163.com
.png)
