肝细胞癌(HCC)已成为世界上最恶性的肿瘤之一,是一种高度致命的癌症。环状RNA (circRNAs)是一种具有闭环结构的非编码RNA,通过作为miRNA的分子海绵或与蛋白质结合来调节生物过程,也参与细胞增殖、分化、凋亡、侵袭等。circRNA可被包裹成外泌体,参与细胞间信号传递,促进多种肿瘤的恶性进展。CD8+T细胞功能障碍是肝细胞癌(HCC)免疫逃逸的主要因素。然而,外泌体来源的环状RNA对CD8+T细胞功能障碍的影响有待进一步探索。

circCCAR1在HCC组织中高表达
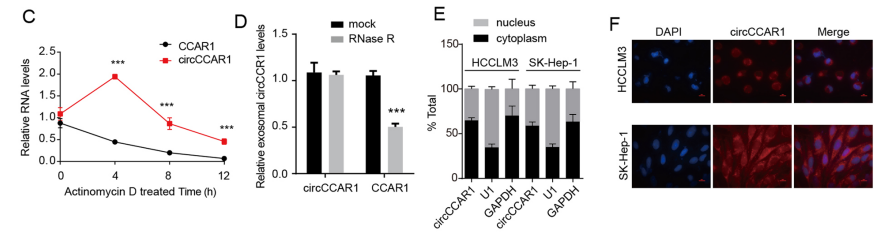
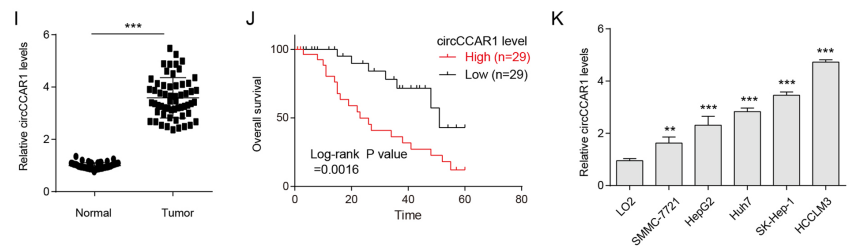
图1 circCCAR1在HCC组织中高表达
circCCAR1在体内外均促进HCC的生长
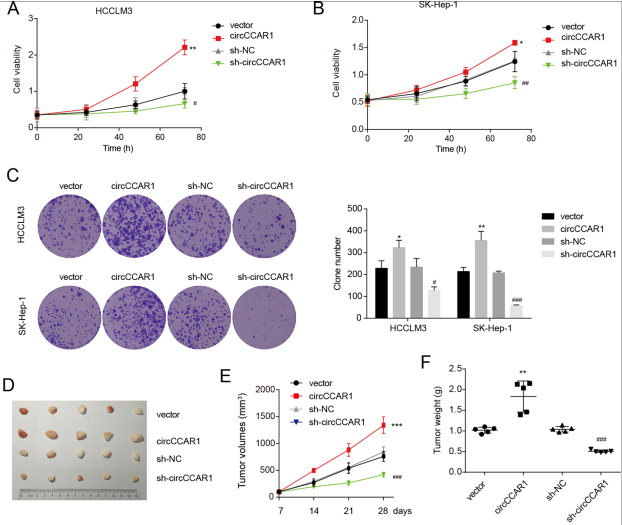
图2 circCCAR1在体内外均促进HCC的生长
circCCAR1在体内外均能促进HCC的转移
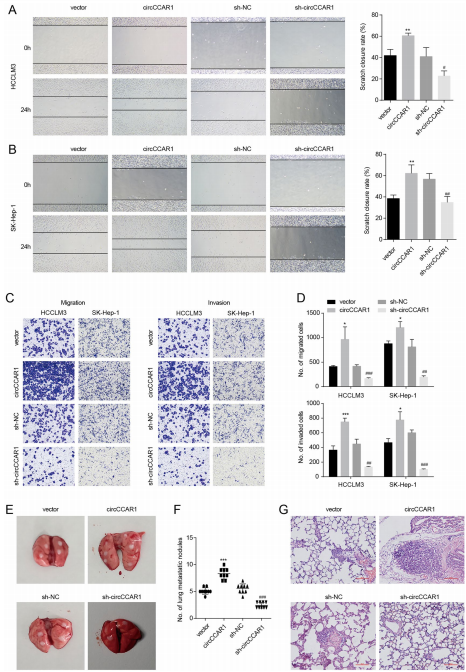
图3 circCCAR1在体内外均能促进HCC的转移
EP300介导的H3K27ac促进HCC中circCCAR1的表达
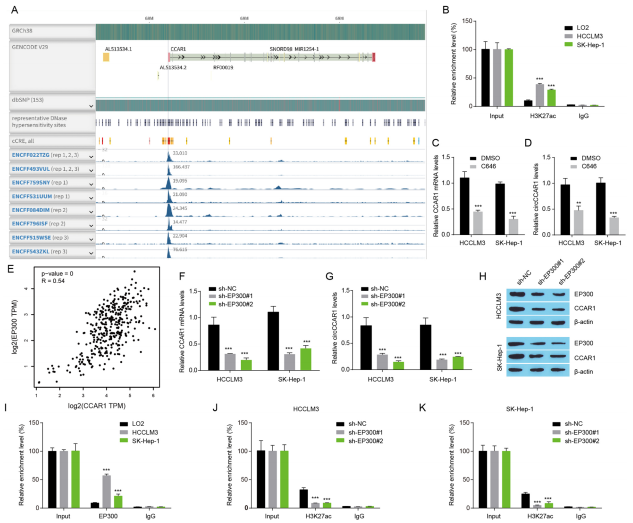
图4 EP300介导的H3K27ac促进HCC中circCCAR1的表达
EIF4A3促进circCCAR1的生成
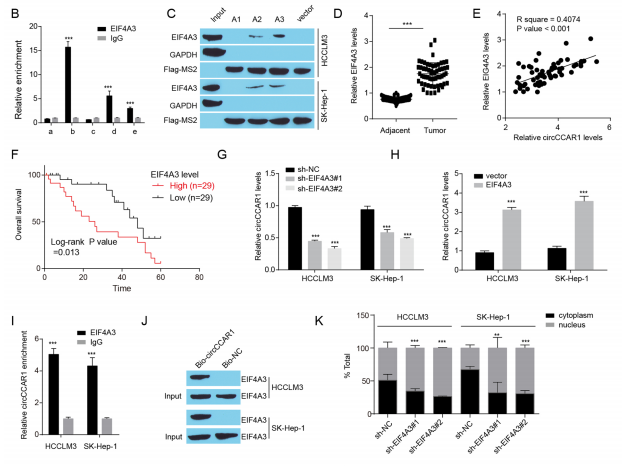
图5 EIF4A3促进circCCAR1的生成
WTAP介导的m6A修饰通过IGF2BP3增强了circCCAR1的稳定性
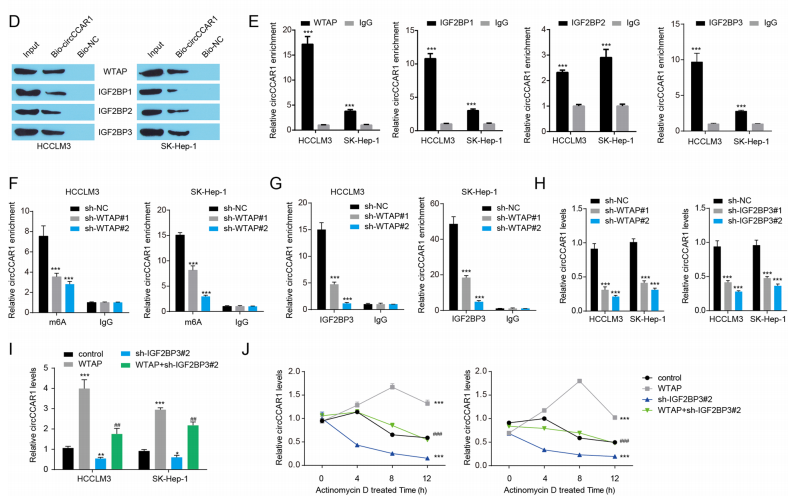
图6 WTAP介导的m6A修饰通过IGF2BP3增强了circCCAR1的稳定性
hnRNPA2B1介导的circCCAR1包装成外泌体
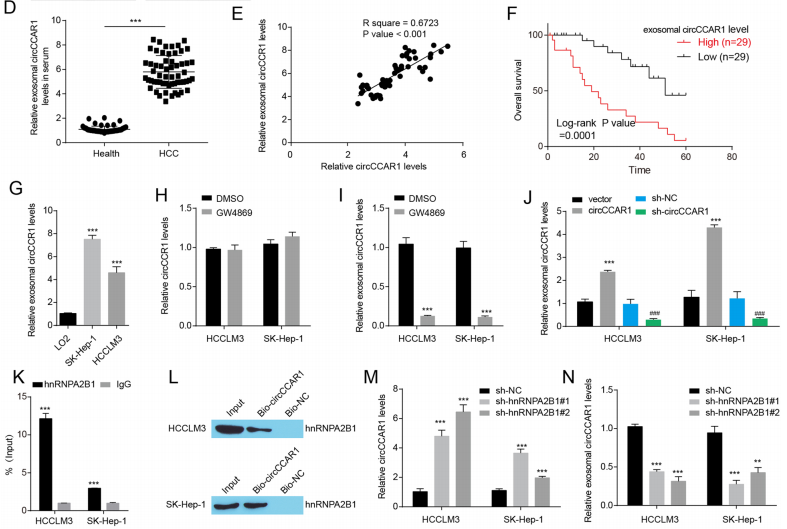
图7 hnRNPA2B1介导的circCCAR1包装成外泌体
外泌体circCCAR1加速抗肿瘤CD8 + T细胞的衰竭
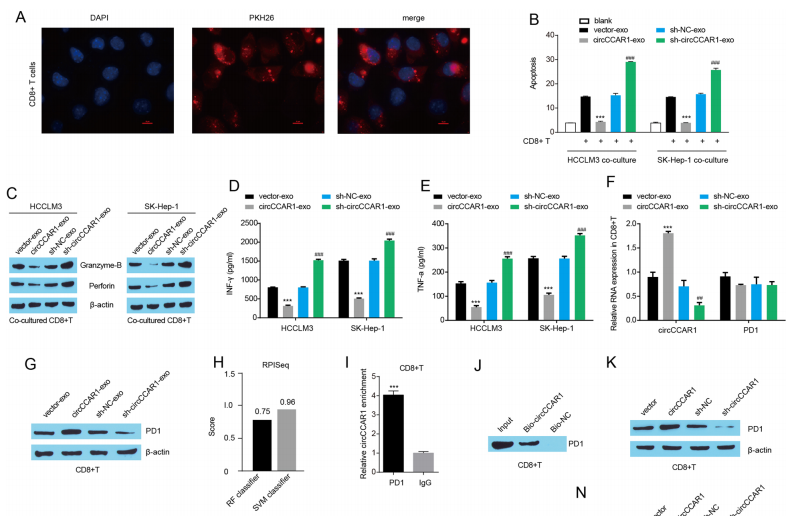
图8 外泌体circCCAR1加速抗肿瘤CD8 + T细胞的衰竭
circCCAR1促进HCC对anti-PD1治疗的耐药性
为了探讨circCCAR1在anti-PD1治疗中的作用,我们构建了HuNSG小鼠异种移植模型。研究发现,携带过表达circCCAR1细胞的HuNSG小鼠外周血外泌体circCCAR1增加,CD8+T细胞低于对照组(图9B)。circCCAR1高表达的异种移植小鼠对PD1治疗有耐药性,生存时间更短。综上所述,circCCAR1促进了HCC的anti-PD1治疗耐药性。
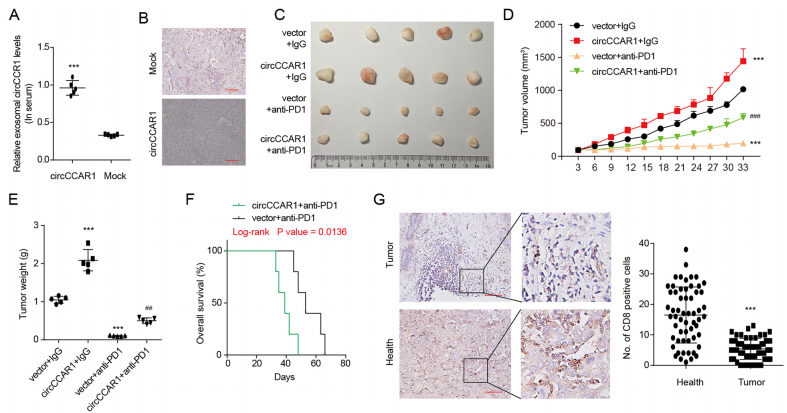
图9 circCCAR1促进HCC对anti-PD1治疗的耐药性
总结
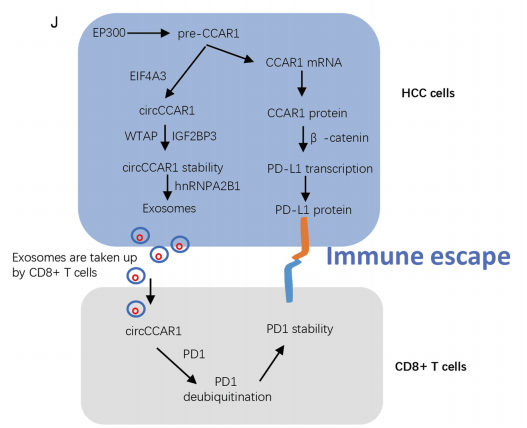
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-023-01759-1
转载请联系邮箱授权:circRNA@163.com
.png)
