
缺氧诱导的circINSIG1在CRC中的特征和临床意义

图1 缺氧诱导的circINSIG1在CRC中的特征和临床意义
circINSIG1编码一个含有121个氨基酸的蛋白
接着,作者为了确定circINSIG1的蛋白编码能力,通过circRNADb数据库分析发现,circINSIG1序列中包含一个可能编码121个氨基酸蛋白(以下简称circINSIG1-121)和一个207-292nt的IRES元件;circINSIG1可以在核糖体单体和多聚体组分中检测到,以及双荧光素酶验证IRES具有高活性初步验证circINSIG1具有翻译多肽的能力。随后作者构建circINSIG1-Flag载体转染CRC细胞进行验证,证实了circINSIG1-121蛋白的内源性存在。接下来,作者通过IHC和WB分析,发现circINSIG1-121蛋白在CRC组织中表达上调,而INSIG1蛋白水平在对应的癌旁组织与CRC组织中无显著差异,并且较高的circINSIG1-121蛋白表达与较差的生存率相关。作者综合研究结果和TCGA数据库信息发现,线性INSIG1的表达水平与CRC患者的生存率没有相关性。总之,circINSIG1编码了一个121个氨基酸的新蛋白,与CRC的不良预后相关。
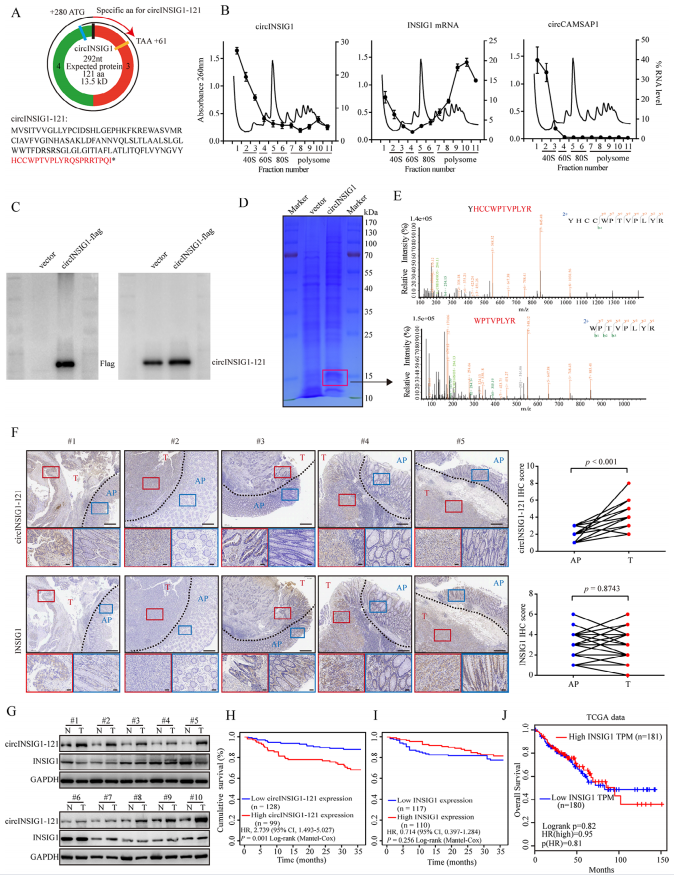
图2 circINSIG1编码一个含有121个氨基酸的蛋白
circINSIG1-121可促进结直肠癌的增殖和转移

图3 circINSIG1-121可促进结直肠癌的增殖和转移
circINSIG1-121与INSIG1相互作用,促进INSIG1的泛素依赖性降解以诱导胆固醇的生物合成

图4 circINSIG1-121与INSIG1相互作用,促进INSIG1的泛素依赖性降解,从而诱导胆固醇的生物合成
circINSIG1-121招募CUL5-ASB6复合物以促进与K48相连的INSIG1泛素化

图5 circINSIG1-121招募CUL5-ASB6复合物,促进INSIG1的泛素化
缺氧诱导的EIF4A3促进circINSIG1的表达
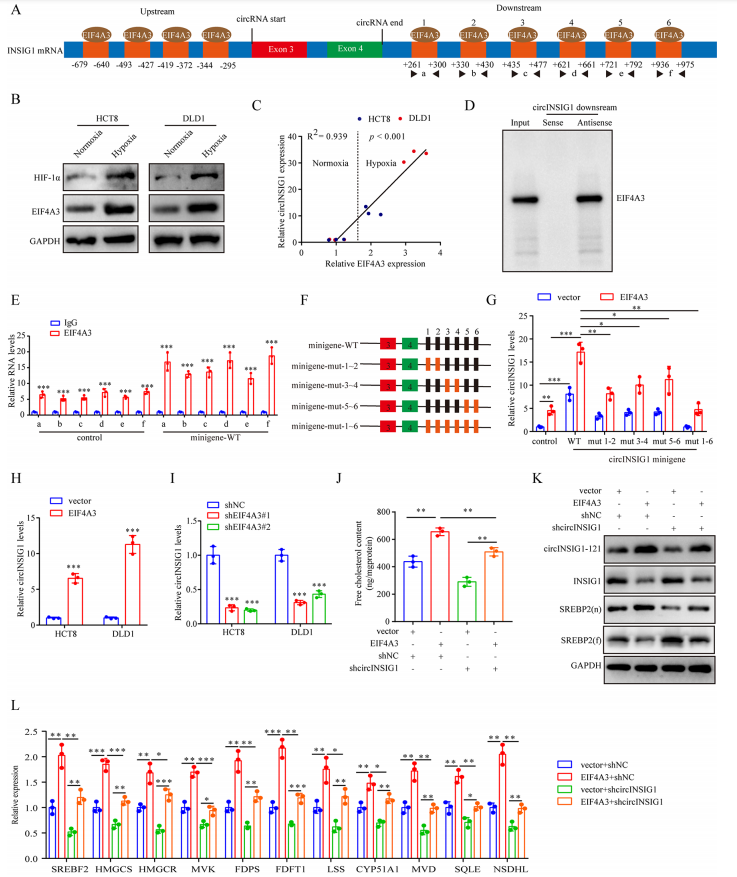
图6 缺氧诱导的EIF4A3促进circINSIG1的表达
circINSIG1是CRC患者潜在的治疗靶点
作者分析了六个患者来源的异种移植(PDX)模型中circINSIG1和circINSIG1-121的表达,选择circINSIG1上调的PDX3和PDX6来检测其治疗效果。用shcircINSIG1慢病毒治疗后,肿瘤生长速度明显慢于对照组。IHC分析显示,在shcircINSIG1慢病毒处理组中,Ki67阳性细胞的百分比显著降低。作者进一步验证了circINSIG1在体内的作用机制,下调circINSIG1降低了circINSIG1-121蛋白水平,并抑制了INSIG1介导的SREBP1信号转导。此外,在circINSIG1敲低的PDX肿瘤中,游离胆固醇含量降低。综上所述,circINSIG1是CRC患者的一个新的潜在治疗靶点。

图7 circINSIG1是CRC患者潜在的治疗靶点
总结
缺氧诱导了circINSIG1的上调,而circINSIG1的生物发生受到EIF4A3的调控。circINSIG1编码一种新的蛋白circINSIG1-121,该蛋白招募CUL5-ASB6复合物,促进关键胆固醇代谢调节因子INSIG1在赖氨酸156和158处的K48连接泛素化,从而促进胆固醇生物合成和CRC进展。circINSIG1提出了一种表观遗传机制,为缺氧和胆固醇代谢之间的关系提供了新的见解,并为CRC的治疗提供了一个很有前途的潜在治疗靶点。
.png)

